
| 实验方案 (只要求填写选用试剂的序号) | 实验现象 | 结论 | |
| (1) | 一支试管中有白色沉淀,另一支试管中先生成白色沉淀,后白色沉淀消失. | 金属性:Mg>Al | |
| (2) | 非金属性: | ||
| 实验方案 (填写选用试剂序号) | 实验现象 | 结论 | |
| (1) | ④⑤⑦ | 一支试管中有白色沉淀生成,另一支试管中先生成白色沉淀,后白色沉淀消失 | 金属性:Mg>Al |
| (2) | ③⑥ | 溶液由无色变为黄色(或橙黄) | 非金属性:Cl>Br |


 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:
| A、1mol CH4含有的电子数为NA |
| B、标准状况下,2.24L的CCl4中含有的氯原子数为0.4NA |
| C、常温常压下,3.0g葡萄糖和冰醋酸的混合物中含有的原子总数为0.4NA |
| D、标准状况下,2.24L的乙炔含碳原子数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

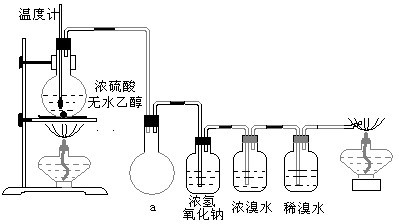
| Cl2 |
| 红磷(少量) |
 ,
, +RCl→
+RCl→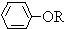 +NaCl
+NaCl查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| X | 其中一种放射性同位素,可用于一些文物或化石的年代测定 |
| Z | 无最高正化合价,其最低负化合价为-2 |
| W | 存在质量数为25,中子数为13的核素 |
| R | 位于周期表第13列 |
| P | 与Z互不同族,且最高价氧化物对应水化物为强酸 |
| 化合物 | WZ | R2Z3 | WP2 | RP3 |
| 晶体类型 | ||||
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com