
”¾ĢāÄæ”æĄ±½·µÄĪ¶µĄÖ÷ŅŖŌ“×ŌÓŚĖłŗ¬µÄĄ±½·ĖŲ£¬¾ßÓŠĻūŃ×”¢ÕņĶ“”¢Āé×ķŗĶ½ä¶¾µČ¹¦Š§£¬ĢŲ±šŹĒĘäÕņĶ“×÷ÓĆÓėĀš·ČĻąČōĒŅ±ČĀš·Čøü³Ö¾Ć”£Ą±½·ĖŲ(F)µÄ½į¹¹¼ņŹ½ĪŖ £¬ĘäŗĻ³ÉĀ·ĻßČēĻĀ£ŗ
£¬ĘäŗĻ³ÉĀ·ĻßČēĻĀ£ŗ

ŅŃÖŖ£ŗR-OH![]() R-Br R-Br+R”Æ-Na
R-Br R-Br+RӮ-Na ![]() RӮ-R+NaBr
RӮ-R+NaBr
»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)Ą±½·ĖŲµÄ·Ö×ÓŹ½ĪŖ___________£¬AĖłŗ¬¹ŁÄÜĶŵÄĆū³ĘŹĒ___________£¬DµÄ×ī¼ņµ„Ķ¬ĻµĪļµÄĆū³ĘŹĒ___________£»
(2)A”śBµÄ·“Ó¦ĄąŠĶĪŖ___________£¬Š“³öC”śDµÄ»Æѧ·½³ĢŹ½___________£»
(3)Š“³öĶ¬Ź±·ūŗĻĻĀĮŠČżøöĢõ¼žµÄDµÄĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½£ŗ___________£»
¢ŁÄÜŹ¹äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗĶŹÉ«
¢ŚÄÜ·¢ÉśĖ®½ā·“Ó¦£¬²śĪļÖ®Ņ»ĪŖŅŅĖį
¢ŪŗĖ“Ź²ÕńĒāĘ×ĪŖČż×é·å£¬ĒŅ·åĆ껿±ČĪŖ3©U2©U1
(4)4£ĪģĻ©Ėį(CH2=CHCH2CH2COOH)æÉÓĆ×÷Å©Ņ©”¢Ņ½Ņ©ÖŠ¼äĢ唣²ĪÕÕŅŌÉĻŗĻ³ÉĀ·Ļߣ¬Éč¼ĘÓÉCH2=CHCH2OHĪŖĘšŹ¼ŌĮĻÖʱø4£ĪģĻ©ĖįµÄŗĻ³ÉĀ·Ļß___________”£
”¾“š°ø”æC18H27O3N Ģ¼Ģ¼Ė«¼ü”¢äåŌ×Ó ±ūĻ©Ėį Č”“ś·“Ó¦ (CH3)2CHCH=CH(CH2)3CH(COOH)2![]() (CH3)2CHCH=CH(CH2)4COOH+CO2”ü
(CH3)2CHCH=CH(CH2)4COOH+CO2ӟ 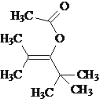 CH2=CHCH2OH
CH2=CHCH2OH![]() CH2=CHCH2Br
CH2=CHCH2Br![]() CH2=CHCH2CH(COOCH2CH3)2
CH2=CHCH2CH(COOCH2CH3)2![]() CH2=CHCH2CH(COOH)2
CH2=CHCH2CH(COOH)2![]() CH2=CHCH2CH2COOH
CH2=CHCH2CH2COOH
”¾½āĪö”æ
øł¾Ż¼üĻߏ½Š“³ö·Ö×ÓŹ½£¬ÕŅ³ö¹ŁÄÜĶÅ£»½įŗĻ”°ŅŃÖŖ”±ŗĶĮ÷³ĢÖŠµÄŠÅĻ¢£¬ŅĄ“ĪČ·¶ØA”¢B”¢C”¢DµÄ½į¹¹¼ņŹ½£¬×ŪŗĻD”¢F½į¹¹æɵĆE½į¹¹¼ņŹ½”£ŌŚ“Ė»ł“”ÉĻ»Ų“šÓŠ¹ŲĪŹĢā”£
øł¾ŻĢāøų”°ŅŃÖŖ”±ŗĶĮ÷³ĢŅŌ¼°DµÄ·Ö×ÓŹ½£¬½ĻŅ×ĶʶĻ³öŗĻ³ÉĀ·ĻßÖŠø÷ĪļÖŹµÄ½į¹¹¼ņŹ½£ŗ
A£ŗ(CH3)2CHCH=CH(CH2)3Br£¬B£ŗ(CH3)2CHCH=CH(CH2)3CH(COOCH2CH3)2£¬
C£ŗ(CH3)2CHCH=CH(CH2)3CH(COOH)2£¬D£ŗ(CH3)2CHCH=CH(CH2)4COOH£¬
E£ŗ(CH3)2CHCH=CH(CH2)4COCl”£
(1)¼üĻߏ½µÄ¶Ėµć”¢×ŖÕŪµć¾łÓŠĢ¼Ō×Ó£¬¾ŻĢ¼4¼ŪŌŌņČ·¶ØĒāŌ×ÓŹż£¬Ą±½·ĖŲµÄ·Ö×ÓŹ½ĪŖC18H27O3N£»ÓÉ”°ŅŃÖŖ”±ŠÅĻ¢£¬ŗĻ³ÉµŚŅ»²½¼“ŌĮĻÖŠōĒ»ł±»äåŌ×ÓČ”“ś£¬AĖłŗ¬¹ŁÄÜĶÅŹĒĢ¼Ģ¼Ė«¼ü”¢äåŌ×Ó£»DµÄĶ¬ĻµĪļ±ŲŠėÓŠ1øöĢ¼Ģ¼Ė«¼üŗĶ1øöōČ»ł£¬DµÄ×ī¼ņµ„Ķ¬ĻµĪļĪŖCH2=CHCOOH£¬Ćū³ĘŹĒ±ūĻ©Ėį”£
(2)ÓÉ”°ŅŃÖŖ”±ŠÅĻ¢£¬A”śBµÄ·“Ӧɜ³ÉNaBr£¬ŌĮĻÖŠĘäÓą²æ·ÖĮ¬½ÓÉś³ÉB£¬ĪŖČ”“ś·“Ó¦”£B”śCĪŖõ„µÄĖ®½ā·“Ó¦£¬æɵĆCµÄ½į¹¹¼ņŹ½ĪŖ(CH3)2CHCH=CH(CH2)3CH(COOH)2”£C”śDĪŖĶŃōČ·“Ó¦£¬Ęä»Æѧ·½³ĢŹ½ĪŖ(CH3)2CHCH=CH(CH2)3CH(COOH)2![]() (CH3)2CHCH=CH(CH2)4COOH+CO2”ü£»
(CH3)2CHCH=CH(CH2)4COOH+CO2”ü£»
(3)D·Ö×ÓŹ½ĪŖC10H18O2£¬²»±„ŗĶ¶ČĪŖ2”£Āś×ćĢāøųĢõ¼žµÄDµÄĶ¬·ÖŅģ¹¹Ģåŗ¬ÓŠĢ¼Ģ¼Ė«¼ü”¢CH3COO-”¢3ÖÖHŌ×ӣطֱš9”¢6”¢3øö£©”£Ó¦ÓŠČżÖÖ¼×»ł£¬ø÷3”¢2”¢1øö£¬ĒŅĶ¬ÖÖ¼×»łĮ¬ŌŚĶ¬Ņ»Ģ¼Ō×ÓÉĻ»ņ“¦ÓŚ·Ö×Ó¶Ō³ĘĪ»ÖĆ”£·ūŗĻĢāŅāµÄĶ¬·ÖŅģ¹¹ĢåĪŖ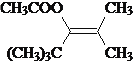 ”£
ӣ
(4)ÓÉCH2=CHCH2OHĪŖĘšŹ¼ŌĮĻŗĻ³ÉCH2=CHCH2CH2COOH£¬·Ö×ÓÖŠŌö¼Ó2øöĢ¼Ō×Ó”£Į÷³ĢÖŠA”śB”śC”śD·Ö×ÓÖŠ¾»Ōö2øöĢ¼Ō×Ó£¬¹ŹÖ±½ÓÄ£·ĀŠ“³öÖʱø4£ĪģĻ©ĖįµÄŗĻ³ÉĀ·Ļߣŗ
CH2=CHCH2OH![]() CH2=CHCH2Br
CH2=CHCH2Br![]() CH2=CHCH2CH(COOCH2CH3)2
CH2=CHCH2CH(COOCH2CH3)2
![]() CH2=CHCH2CH(COOH)2
CH2=CHCH2CH(COOH)2![]() CH2=CHCH2CH2COOHӣ
CH2=CHCH2CH2COOHӣ


 Ē§ĄļĀķ×ßĻņ¼ŁĘŚĘŚÄ©·ĀÕęŹŌ¾ķŗ®¼ŁĻµĮŠ“š°ø
Ē§ĄļĀķ×ßĻņ¼ŁĘŚĘŚÄ©·ĀÕęŹŌ¾ķŗ®¼ŁĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŃŠ¾æ»Æѧ·“Ó¦Ź±£¬¼ČŅŖæ¼ĀĒĪļÖŹ±ä»ÆÓėÄÜĮæ±ä»Æ£¬ÓÖŅŖ¹Ų×¢·“Ó¦µÄæģĀżÓėĻŽ¶Č”£»Ų“šĻĀĮŠĪŹĢā£ŗ
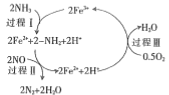
(1)NH3»¹ŌNOŹĒÖŲŅŖµÄŃĢĘųĶŃĻõ¼¼Źõ£¬Ęä·“Ó¦¹ż³ĢÓėÄÜĮæ¹ŲĻµČēĻĀĶ¼ĖłŹ¾”£

¢ŁÉĻĶ¼ÖŠŅņĪŖøıäĮĖ·“Ó¦Ģõ¼ž£¬·“Ó¦µÄ»ī»ÆÄÜb___________(Ģī”°£¾”±”°£¼”±»ņ”°£½”±)a”£
¢ŚĶŃĻõ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ·“Ó¦Īļ”śÉś³ÉĪļ”÷H£½___________(ÓĆE1£¬ E2µÄ“śŹżŹ½±ķŹ¾)
¢ŪŃŠ¾æ·¢ĻÖ£¬Ņ»¶ØĢõ¼žĻĀµÄĶŃĻõ·“Ó¦¹ż³ĢæÉÄÜČēĶ¼ĖłŹ¾£¬øł¾ŻŃõ»Æ»¹Ō·“Ó¦ÖŠĪļÖŹµÄ×÷ÓĆ£¬NOĪŖ¼Į____£¬ĶŃĻõ×Ü·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ___________”£
(2)Ņ»¶ØĪĀ¶ČĻĀ£¬½«²»Ķ¬ĪļÖŹµÄĮæµÄH2O(g)ŗĶCO·Ö±šĶØČėČŻ»żĪŖ1LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ£¬½ųŠŠ·“Ó¦H2O(g)+CO(g)£½CO2(g)+H2(g)£¬µĆµ½Čē±ķĖłŹ¾µÄČż×鏿¾Ż£ŗ
ŹµŃ鱹ŗÅ | ĪĀ¶Č/”ę | ĘšŹ¼Įæ/mol | Ę½ŗāĮæ/mol | “ļµ½Ę½ŗāĖłŠčŹ±¼ä/min | ||
H2O(g) | CO(g) | CO(g) | H2(g) | |||
1 | 650 | 2.0 | 4.0 | 3.0 | 1.0 | 5 |
2 | 900 | 1.0 | 2.0 | 1.8 | 0.2 | 4 |
3 | 900 | a | b | c | d | t |
¢ŁŹµŃé2£ŗ4min
¢Ś650”ꏱ£¬ČōŌŚ“ĖČŻĘ÷ÖŠ³äČė2.0molH2O(g)”¢1.0molCO(g)”¢1.0molCO2(g)ŗĶxmolH2(g)£¬ŅŖŹ¹·“Ó¦ŌŚæŖŹ¼Ź±¼äĻņÕż·“Ó¦·½Ļņ½ųŠŠ£¬ŌņxÓ¦Āś×ćµÄĢõ¼žŹĒ___________”£
¢ŪČōa=2.0£¬b=1.0£¬ŌņĘ½ŗāŹ±ŹµŃé2ÖŠH2O(g)ŗĶŹµŃé3ÖŠCO(g)µÄ×Ŗ»ÆĀŹ(¦Į)µÄ¹ŲĻµĪŖ¦Į(H2O)___________(Ģī”°£¾”±”°£¼”±»ņ”°=”±)¦Į(CO)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ×ī»īĘĆµÄ½šŹōŌŖĖŲ”¢×ī»īĘƵķĒ½šŹōŌŖĖŲ”¢³£ĪĀĻĀ³ŹŅŗĢ¬µÄ½šŹō(¼Ūµē×ÓÅŲ¼ĪŖ5d106s2)ŌŖĖŲ·Ö±šĪ»ÓŚĻĀĆęŌŖĖŲÖÜĘŚ±ķÖŠµÄ(””””)
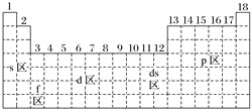
A. sĒų”¢pĒų”¢dsĒų B. sĒų”¢pĒų”¢dĒų
C. fĒų”¢pĒų”¢dsĒų D. sĒų”¢fĒų”¢dsĒų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĒÅ»·ĶéĢžŹĒÖø¹²ÓĆĮ½øö»ņĮ½øöŅŌÉĻĢ¼Ō×ӵĶą»·ĶéĢž£¬¶ž»·[1£¬1£¬0]¶”Ķé(![]() )ŹĒ×ī¼ņµ„µÄŅ»ÖÖ”£ĻĀĮŠ¹ŲÓŚøĆ»ÆŗĻĪļµÄĖµ·Ø“ķĪóµÄŹĒ
)ŹĒ×ī¼ņµ„µÄŅ»ÖÖ”£ĻĀĮŠ¹ŲÓŚøĆ»ÆŗĻĪļµÄĖµ·Ø“ķĪóµÄŹĒ
A. Óė1£¬3-¶”¶žĻ©»„ĪŖĶ¬·ÖŅģ¹¹Ģå
B. ¶žĀČ“śĪļ¹²ÓŠ4ÖÖ
C. Ģ¼Ģ¼¼üÖ»ÓŠµ„¼üĒŅ±Ė“ĖÖ®¼äµÄ¼Š½ĒÓŠ45”ćŗĶ90”ćĮ½ÖÖ
D. ĆæŅ»øöĢ¼Ō×Ó¾ł“¦ÓŚÓėĘäÖ±½ÓĻąĮ¬µÄŌ×Ó¹¹³ÉµÄĖÄĆęĢåÄŚ²æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪåÖÖÖ÷×åŌŖĖŲX”¢Y”¢Z”¢MŗĶNŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A. MµÄŌ×Ó°ė¾¶±ČNŠ”
B. YŗĶZ¼ČæÉŠĪ³ÉZ2Y£¬Ņ²æÉŠĪ³ÉZ2Y2
C. X2MµÄČČĪČ¶ØŠŌ±ČX2YĒæ
D. MŗĶNµÄŃõ»ÆĪļµÄĖ®»ÆĪļ¾łĪŖĒæĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗćĪĀ25”ęĻĀ£¬ĻņŅ»¶ØĮæµÄ0.1mol/LµÄBOHČÜŅŗÖŠÖšµĪµĪČėĻ”ŃĪĖį”£ČÜŅŗÖŠĖ®µēĄė³öµÄĒāĄė×ÓÅØ¶ČµÄøŗ¶ŌŹż[ÓĆpC±ķŹ¾£¬pC=-1gc(H+)Ė®]Óė¼ÓČėŃĪĖįĢå»żµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠŠšŹö“ķĪóµÄŹĒ£Ø £©

A. BOHĪŖČõ¼īĒŅKbµÄŹżĮ漶ĪŖ10”Ŗ5
B. bµćČÜŅŗ³ŹÖŠŠŌ
C. c-dµć¼äČÜŅŗÖŠ£ŗc(BOH)+c(OH”Ŗ)>c(H+)
D. cµćČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Č×ī“ó£¬ĒŅc(B+)<c(Cl”Ŗ)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻõ±½µŲĘ½HŹĒŅ»ÖÖÖĪĮĘøßŃŖŃ¹µÄŅ©Īļ£»ĘäŅ»ÖÖŗĻ³ÉĀ·ĻßČēĻĀ£ŗ

ŅŃÖŖ£ŗõ„·Ö×ÓÖŠµÄa-Ģ¼Ō×ÓÉĻµÄĒā±Č½Ļ»īĘĆ£¬Ź¹õ„Óėõ„Ö®¼äÄÜ·¢ÉśĖõŗĻ·“Ó¦”£
![]()
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©BµÄ»ÆѧĆū³ĘĪŖ________£®
£Ø2£©¢ŚµÄ·“Ó¦ĄąŠĶŹĒ________£®
£Ø3£©DµÄ½į¹¹¼ņŹ½ĪŖ________£®
£Ø4£©HµÄ·Ö×ÓŹ½ĪŖ________£®
£Ø5£©·“Ó¦¢ŁµÄ»Æѧ·½³ĢŹ½ĪŖ________£®
£Ø6£©ŅŃÖŖMÓėG»„ĪŖĶ¬·ÖŅģ¹¹Ģ壬MŌŚŅ»¶ØĢõĢåĻĀÄÜ·¢ÉśŅų¾µ·“Ó¦£¬ŗĖ“Ź²ÕńĒāĘ×ĻŌŹ¾ÓŠ4×é·å£¬·åĆ껿֮±ČĪŖ1:1:2:4£¬Š“³öMµÄŅ»ÖÖæÉÄܵĽį¹¹¼ņŹ½________£®
£Ø7£©ĄĪ÷µŲĘ½ Ņ²ŹĒŅ»ÖÖÖĪĮĘøßŃŖŃ¹Ņ©Īļ£¬ÉčŅŌŅŅ“¼ŗĶ
Ņ²ŹĒŅ»ÖÖÖĪĮĘøßŃŖŃ¹Ņ©Īļ£¬ÉčŅŌŅŅ“¼ŗĶ ĪŖŌĮĻÖʱøĄĪ÷µŲĘ½µÄŗĻ³ÉĀ·Ļß(ĪŽ»śŹŌ¼ĮČĪŃ”)”£________________________
ĪŖŌĮĻÖʱøĄĪ÷µŲĘ½µÄŗĻ³ÉĀ·Ļß(ĪŽ»śŹŌ¼ĮČĪŃ”)”£________________________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潚Źō¼°Ęä»ÆŗĻĪļŌŚČĖĄąÉś»ī”¢Éś²śÖŠ·¢»Ó×ÅÖŲŅŖµÄ×÷ÓĆ£®
£Ø1£©ĢśŹĒČĖĄąÓ¦ÓĆ×ī¹ćµÄ½šŹō£¬¹¤ŅµÉĻÓĆĢśæóŹÆ£ØÖ÷ŅŖ³É·ÖĪŖFe2O3 £©”¢½¹Ģ攢ŹÆ»ŅŹÆŌŚøßĀÆÖŠŅ±Į¶µĆµ½£¬øßĀÆĮ¶ĢśµÄÖ÷ŅŖ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ__________________ £¬ĘäÖŠŹÆ»ŅŹÆµÄ×÷ÓĆŹĒ____________________ ”£
£Ø2£©ĀĮŹĒ³£¼ūµÄ½šŹō£¬ĀĮÖĘČŻĘ÷¼Č²»ÄÜ“ę·ÅĖįŠŌĪļÖŹ£¬Ņ²²»ÄÜ“ę·Å¼īŠŌĪļÖŹ£¬ĘäŌŅņ·Ö±šÓĆĄė×Ó·½³ĢŹ½±ķŹ¾£ŗ_____________”¢ _____________ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøß“æĮņĖįĆĢ×÷ĪŖŗĻ³ÉÄųīÜĆĢČżŌŖÕż¼«²ÄĮĻµÄŌĮĻ£¬¹¤ŅµÉĻæÉÓÉĢģČ»¶žŃõ»ÆĆĢ·ŪÓėĮņ»ÆĆĢæó£Ø»¹ŗ¬Fe”¢Al”¢Mg”¢Zn”¢Ni”¢SiµČŌŖĖŲ£©Öʱø£¬¹¤ŅÕČēĻĀĶ¼ĖłŹ¾”£»Ų“šĻĀĮŠĪŹĢā£ŗ

Ļą¹Ų½šŹōĄė×Ó[c0(Mn+)=0.1 mol”¤L1]ŠĪ³ÉĒāŃõ»ÆĪļ³ĮµķµÄpH·¶Ī§ČēĻĀ£ŗ
½šŹōĄė×Ó | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
æŖŹ¼³ĮµķµÄpH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
³ĮµķĶźČ«µÄpH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
£Ø1£©”°ĀĖŌü1”±ŗ¬ÓŠSŗĶ__________________________£»Š“³ö”°Čܽž”±ÖŠ¶žŃõ»ÆĆĢÓėĮņ»ÆĆĢ·“Ó¦µÄ»Æѧ·½³ĢŹ½____________________________________________________”£
£Ø2£©”°Ńõ»Æ”±ÖŠĢķ¼ÓŹŹĮæµÄMnO2µÄ×÷ÓĆŹĒ½«________________________”£
£Ø3£©”°µ÷pH”±³żĢśŗĶĀĮ£¬ČÜŅŗµÄpH·¶Ī§Ó¦µ÷½ŚĪŖ_______~6Ö®¼ä”£
£Ø4£©”°³żŌÓ1”±µÄÄæµÄŹĒ³żČ„Zn2+ŗĶNi2+£¬”°ĀĖŌü3”±µÄÖ÷ŅŖ³É·ÖŹĒ______________”£
£Ø5£©”°³żŌÓ2”±µÄÄæµÄŹĒÉś³ÉMgF2³Įµķ³żČ„Mg2+”£ČōČÜŅŗĖį¶Č¹żøߣ¬Mg2+³Įµķ²»ĶźČ«£¬ŌŅņŹĒ_____________________________________________________________________”£
£Ø6£©Š“³ö”°³ĮĆĢ”±µÄĄė×Ó·½³ĢŹ½___________________________________________________”£
£Ø7£©²ćדÄųīÜĆĢČżŌŖ²ÄĮĻæÉ×÷ĪŖļ®Ąė×Óµē³ŲÕż¼«²ÄĮĻ£¬Ęä»ÆѧŹ½ĪŖLiNixCoyMn![]() Ź±£¬z=___________”£
Ź±£¬z=___________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com