
【题目】阿立哌唑E(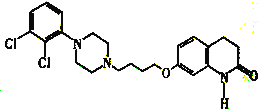 )是新型非典型抗精神病药物,被誉为“多巴胺系统稳定剂”,可由以下路线合成:
)是新型非典型抗精神病药物,被誉为“多巴胺系统稳定剂”,可由以下路线合成:
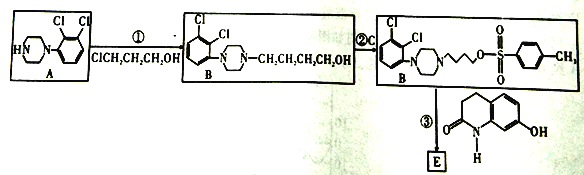
其中C是一种有机强酸。请回答下列问题:
(1)所发生的反应中属于取代反应的是____________(填序号)。
(2)写出B生成D的化学方程式是____________。
(3)E的分子式为____________。
(4)已知F:①与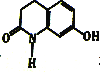 水解的产物互为同分异构体;②属于α一氨基酸;③苯环上有两个取代基;④核磁共振氢谱图中有6个峰;⑤能与FeCl3溶液发生显色反应。F的结构简式为_______。
水解的产物互为同分异构体;②属于α一氨基酸;③苯环上有两个取代基;④核磁共振氢谱图中有6个峰;⑤能与FeCl3溶液发生显色反应。F的结构简式为_______。
(5)已知:R-CHO![]()
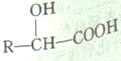 。合成路线流程图示例:
。合成路线流程图示例:
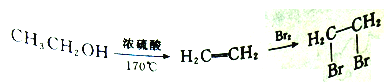
①ClCH2CH2CH2CH2OH的系统命名是_____________。
②写出由ClCH2CH2CH2CH2OH制备化合物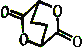 的合成路线流程图(无机试剂任选)。_____________
的合成路线流程图(无机试剂任选)。_____________
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
【题目】游离态碳在自然界存在形式有多种,在工业上有着重要用途。请回答下列问题:
(1)我国四大发明之一的黑火药由木炭与硫黄、硝酸钾按一定比例混合而成。黑火药爆炸时生成硫化钾、氮气和二氧化碳。其爆炸的化学方程式为_____________________________________。
(2)高级碳粉可由烃类高温分解而制得,已知几个反应的热化学方程式:
C(s)+O2(g)==CO2(g) △H1= -393.5 kJmol-1
2H2(g)+O2(g)=2H2O(1) △H2= -571.6 kJmol-1
CH4(g)+2O2(g)-=CO2(g)+ 2H2O(1) △H3= -890.3 kJmol-1
则由天然气生产高级碳粉的热化学方程式为__________________________________。
(3)活性炭可以用来净化气体和液体。
①用活性炭还原氮氧化物,可防止空气污染。向1L闭容器加入一定量的活性炭和NO,某温度下发生反应C(s)+2NO(g)![]() N2(g)+CO2(g),测得不同时间内各物质的物质的量如下表:
N2(g)+CO2(g),测得不同时间内各物质的物质的量如下表:
物质的量/mol 时间/min | NO | N2 | CO2 |
0 | 0.200 | 0 | 0 |
10 | 0.116 | 0.042 | 0.042 |
20 | 0.080 | 0.060 | 0.060 |
30 | 0.080 | 0.060 | 0.060 |
此温度下,该反应的平衡常数K=________(保留两位小数)。10-20min内,NO的平均反应速率为_______________;若30min后升高温度,达到新平衡时,容器中c(NO)∶c(N2) ∶c(CO2)=2∶1∶1,则该反应的ΔH________0(填“>”、“<”或“=”)。
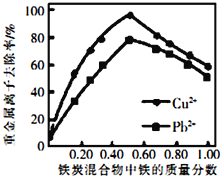
②活性炭和铁屑混合可用于处理水中污染物。在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如图所示。当混合物中铁的质量分数为0时,也能去除水中少量的Cu2+和Pb2+,其原因是_________________;当混合物中铁的质量分数大于50%时,随着铁的质量分数的增加,Cu2+和Pb2+的去除率不升反降,其主要原因是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
IVA 族元素及其化合物在材料等方面有重要用途。回答下列问题:
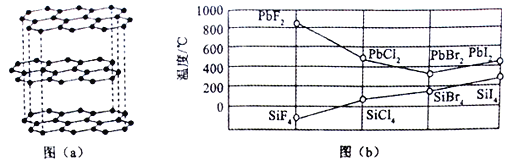
(1)碳的一种单质的结构如图(a)所示。该单质的晶体类型为________________,依据电子云的重叠方式,原子间存在的共价键类型有_____________,碳原子的杂化轨道类型为_________。
(2)石墨烯是从石墨材料中剥离出来的、由单层碳原子组成的二维晶体。将氢气加入到石墨烯中可制得一种新材料石墨烷。下列判断错误的是___________。
A.石墨烯是一种强度很高的材料
B.石墨烯是电的良导体而石墨烷则为绝缘体
C.石墨烯与石墨烷均为高分子化合物
D.石墨烯与H2 制得石墨烷的反应属于加成反应
(3)四卤化硅SiX4的沸点和二卤化铅PbX2 的熔点如图(b)所示。
①SiX4的沸点依F、Cl、Br、I 次序升高的原因是_________________________________。
②结合SiX4的沸点和PbX2的熔点的变化规律,可推断: 依F、Cl、Br、I 次序,PbX2 中的化学键的离子性___________、共价性______________。(填 “增 强”“不变”或“减 弱 ”)
(4)碳的另一种单质C60,晶胞结构与金属铜晶胞相似,其晶胞参数为a nm,晶体密度为_______g·cm-3(只列计算式,不需化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.1mol由两种气态烃组成的混合气体完全燃烧后,得到0.16mol CO2和3.6克水,则混合气体中( )
A. 一定有甲烷
B. 一定是甲烷和乙烯
C. 可能有乙烷
D. 一定有乙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,用一定量的水吸收氨气后制得浓度为12.0 mol·L-1、密度为0.915 g·cm-3的氨水。试计算1体积水吸收多少体积的氨气可制得上述氨水。(本题中氨的式量以 17.0计,氨水的溶质以溶解的NH3为准,水的密度以1.00g·cm-3计)_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个容积相同的容器中,一个盛有HCl气体,另—个盛有H2和Cl2的混合气体。在同温同压下, 两容器内的气体一定具有相同的( )
A. 原子数 B. 密度 C. 质量 D. 质子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是SO2制取、性质检验、收集、尾气处理的装置,有关说法正确的是
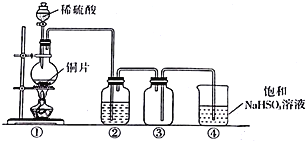
A. 上图中有两处错误
B. 装置①也可以用于制取氨气、氯气
C. 在②中加入品红或紫色石蕊试液都可以验证SO2的漂白性
D. 在②中加入BaCl2溶液,先生成白色沉淀,随后沉淀慢慢消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某硫酸试剂瓶的标签上的部分文字。据此,下列说法正确的是

A. 该试剂中加入适量蒸馏水可以获得较稀的硫酸溶液
B. 该试剂瓶的标签上应印有如图所示的警示标记

C. 该硫酸与等体积水混合所得溶液的物质的量浓度等于9.2mol/L
D. 在50mL量筒中配制0.1000mol/L硫酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3·5H2O)。
I.【查阅资料】
①硫代硫酸钠(Na2S2O3)易溶于水,在中性或碱性环境中稳定,受热、遇酸易分解。
②Na2S2O3·5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成。
③向Na2CO3和Na2S混合溶液中通人SO2可制得Na2S2O3(反应方程式为:![]() ,所得产品常含有少量Na2SO3和Na2SO4。
,所得产品常含有少量Na2SO3和Na2SO4。
Ⅱ.【制备产品】实验装置如图所示:
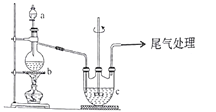
(1)实验步骤:检查装置气密性后,向三颈瓶c中加人Na2CO3和Na2S的混舍溶液,再将分液漏斗a中液体滴加到烧瓶b中加热发生反应产生SO2,请写出b中发生反应的化学方程式________。待Na2S和Na2CO3完全消耗后,结束反应。过滤c中的混合物,滤液经____(填操作名称)、过滤、洗涤、干燥、得到产品。
(2)为了保证硫代硫酸钠的产量,实验中通人的SO2不能过量,原因是_________。
III.【测定产品纯度】
称取10g产品(Na2S2O3·5H2O),配成250mL溶液,取25mL,以淀粉作指示剂,用0.1000mol/L碘的标准溶液滴定。反应原理为:![]() (忽略Na2SO3与I2反应)。
(忽略Na2SO3与I2反应)。
(3)滴定至终点的现象为:____。
(4)重复三次的实验数据如左下表所示,其中第三次读数时滴定管中起始和终点的液面位置如右下图所示,则x=___mL,产品的纯度为____。

IV.【探究与反思】
(5)为验证产品中含有Na2SO3和Na2SO4该小组设计了以下实验方案,请将方案补充完整(所需试剂从稀HN03、稀H2SO4、稀盐酸、蒸馏水中选择):取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,____,则可确定产品中含有Na2SO3和Na2SO4。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com