
常温下,下列各组微粒在指定的溶液中一定能大量共存的是( )
A.加入金属镁产生H2的溶液中:NH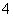 、Na+、SO
、Na+、SO 、CH3COO-
、CH3COO-
B.含有大量ClO-的溶液中:K+、Na+、NO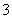 、SO
、SO
C.c(Cu2+)=0.1 mol·L-1的溶液中:H+、NH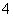 、Br-、CO
、Br-、CO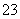
D.含有大量MnO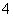 的溶液中:H+、SO
的溶液中:H+、SO 、Cl-、CH3CH2OH
、Cl-、CH3CH2OH
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
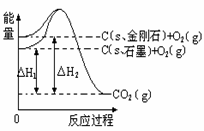
如下图所示,△H1=-393.5 kJ?mol-1,
△H2=-395.4 kJ?mol-1,下列说法或表示式正确的是
A. C(s、石墨)== C(s、金刚石) △H= - 1.9 kJ?mol-1
B. 石墨和金刚石的转化是物理变化
C. 石墨的稳定性强于金刚石
D. 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化硅(Si3N4)是一种优良的高温结构陶瓷,在工业生产和科技领域中有重要用途。
Ⅰ.工业上有多种方法来制备氮化硅,下面是几种常见的方法:
方法一 直接氮化法:在1 300~1 400 ℃时,高纯粉状硅与纯氮气化合,其反应方程式为________________________________________________________________________。
方法二 化学气相沉积法:在高温条件下利用四氯化硅气体、纯氮气、氢气反应生成氮化硅和HCl,与方法一相比,用此法制得的氮化硅纯度较高,其原因是________________________________________________________________________。
方法三 Si(NH2)4热分解法:先用四氯化硅与氨气反应生成Si(NH2)4和一种气体________________(填分子式);然后使Si(NH2)4受热分解,分解后的另一种产物的分子式为____________________。
Ⅱ.(1)氮化硅抗腐蚀能力很强,但易被氢氟酸腐蚀,氮化硅与氢氟酸反应生成四氟化硅和一种铵盐,此盐中存在的化学键类型有______________。
(2)已知:25 ℃,101 kPa条件下的热化学方程式:
3Si(s)+2N2(g)===Si3N4(s) ΔH=-750.2 kJ·mol-1①
Si(s)+2Cl2(g)===SiCl4(g) ΔH=-609.6 kJ·mol-1②
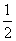 H2(g)+
H2(g)+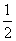 Cl2(g)===HCl(g) ΔH=-92.3 kJ·mol-1③
Cl2(g)===HCl(g) ΔH=-92.3 kJ·mol-1③
请写出四氯化硅气体与氮气、氢气反应的热化学方程式:
________________________________________________________________________。
Ⅲ.工业上制取高纯硅和四氯化硅的生产流程如下:

已知:X、高纯硅、原料B的主要成分都可与Z反应,Y与X在光照或点燃条件下可反应,Z的焰色呈黄色。
(1)原料B的主要成分是________(写名称)。
(2)写出焦炭与原料B中的主要成分反应的化学方程式:
________________________________________________________________________。
(3)上述生产流程中电解A的水溶液时,阳极材料能否用Cu?________(填“能”或“不能”)。写出Cu为阳极电解A的水溶液开始一段时间阴、阳极的电极方程式。
阳极:________;阴极________。
查看答案和解析>>
科目:高中化学 来源: 题型:
向含有Mn2+的酸性溶液中滴加过二硫酸钾(K2S2O8)溶液,会发生如下反应(未配平):Mn2++S2O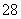 +H2O―→MnO
+H2O―→MnO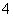 +SO
+SO +H+。下列说法正确的是( )
+H+。下列说法正确的是( )
A.该反应中起氧化作用的是Mn2+
B.反应后溶液的pH降低
C.反应中有1 mol还原剂参加反应,则转移的电子为4 mol
D.该反应常用于检验溶液中Mn2+的存在,现象是溶液紫红色消失
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在指定条件下能大量共存的是( )
①漂白粉的水溶液中:Fe2+、Cl-、Ca2+、Na+ ②滴加石蕊试液呈红色的溶液:K+、NH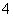 、Cl-、S2- ③能够与金属Cu常温下反应放出气体的溶液:Fe3+、Al3+、SO
、Cl-、S2- ③能够与金属Cu常温下反应放出气体的溶液:Fe3+、Al3+、SO 、K+
、K+
④常温下pH=2的溶液中:NH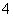 、Na+、Cl-、Cu2+
、Na+、Cl-、Cu2+
⑤无色溶液中:K+、CH3COO-、HCO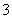 、MnO
、MnO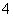
A.②③ B.①③
C.③④ D.①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
食盐中含有一定量的杂质,加碘盐中碘的损失主要是由于杂质、水分、空气中的氧气以及光照、受热而引起的。
已知:①氧化性:IO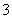 >Fe3+>I2;②KI+I2KI3
>Fe3+>I2;②KI+I2KI3
(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Fe2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为四份。第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。
①向第四份试液中加K3Fe(CN)6溶液,根据是否得到具有特征蓝色沉淀的盐,可检验溶液中是否含有Fe2+,推测该蓝色沉淀是_______
(用化学式表示)。
②第二份试液中加入足量KI固体后,反应的离子方程式为:____________________、____________________。
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失写出潮湿环境下KI与氧气反应的化学方程式:____________________。
将I2溶于KI溶液,在低温条件下,可制得KI3·H2O。该物质不适合作为食盐加碘剂,其理由是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
①氯气的性质活泼,它与氢气混合后立即发生爆炸 ②实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钙溶液吸收 ③新制氯水的氧化性强于久置氯水的
④检验HCl气体中是否混有Cl2,方法是将气体通入硝酸银溶液 ⑤除去HCl气体中的Cl2,可将气体通入饱和食盐水中
A.①②③ B.②③④ C.③ D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是
A.乙醇和乙酸都是常用调味品的主要成分
B.乙醇和乙酸的沸点和熔点都比C2H6、C2H4的沸点和熔点高
C.乙醇和乙酸都能发生取代反应
D.乙醇和乙酸之间能发生酯化反应,酯化反应和皂化反应是可逆反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com