
分析 (1)根据v=$\frac{△c}{△t}$,进行分析求解;
a、改铁片为铁粉,增加接触面积;
b、改稀H2SO4为98%的浓H2SO4,发生钝化;
c、升高温度,反应速率加快;
d、滴加少量CuSO4溶液,构成原电池加快反应速率;
(2)反应Fe+H2SO4=FeSO4+H2↑,是放热反应,所以反应的总能量高于生成物的总能量;
(3)铁是原电池的负极,电解质溶液是硫酸,画出装置图即可.
解答 解:Ⅰ(1)v=$\frac{△c}{△t}$=$\frac{1-0.4}{2}$=0.3mol/(L•min);
a、改铁片为铁粉,增加接触面积,反应速率加快,故不选;
b、改稀H2SO4为98%的浓H2SO4,发生钝化,反应速率减慢,故选;
c、升高温度,反应速率加快,故不选;
d、滴加少量CuSO4溶液,构成原电池加快反应速率,故不选;
故选:0.3mol/(L•min);b;
(2)反应Fe+H2SO4=FeSO4+H2↑,是放热反应,所以反应的总能量高于生成物的总能量,所以体系的能量变化图为: ,故答案为:
,故答案为: ;(3)铁是原电池的负极,电解质溶液是硫酸,原电池的装置图为:
;(3)铁是原电池的负极,电解质溶液是硫酸,原电池的装置图为: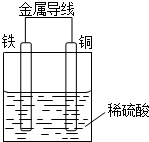 ,故答案为:
,故答案为: .
.
点评 本题考查原电池和电解池知识,侧重于学生的分析能力和电化学知识的综合考查,为高考常见题型和高频考点,注意设计原电池和能量的变化图,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 一定有乙烯 | B. | 一定有甲烷 | C. | 一定没有甲烷 | D. | 一定没有乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸的电离方程式:H2CO3=2H++CO32- | |
| B. | F-的结构示意图: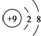 | |
| C. | ${\;}_{55}^{134}$Cs和${\;}_{55}^{137}$Cs形成的单质物理性质相同 | |
| D. | NH3 的电子式: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素非金属性:Z<R | B. | 元素的原子序数:b>a>c>d | ||
| C. | 离子半径bYn+<cZn- | D. | 最高价氧化物对应水化物碱性:X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
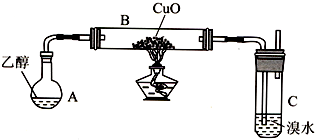
| 试剂、用品 | 预期现象 | |
| 甲 | 酸性高锰酸钾溶液 | 溶液紫红色褪去 |
| 乙 | 溴水 | 溴水褪色 |
| 丙 | 铜丝 酒精灯 | 铜丝由黑色变成光亮的红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制碱性Cu(OH)2悬浊液 | B. | FeCl3溶液 | ||
| C. | BaCl2溶液 | D. | 酸性KMnO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 各物质的浓度之比c(A):c(B):c(C)=2:3:4 | |
| B. | 平衡混合气体中各物质的浓度相等 | |
| C. | 平衡混合气的体积是反应开始前的$\frac{4}{5}$ | |
| D. | 单位时间内,若消耗了a mol A物质,同时也消耗了2a mol C物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④>③>①>② | B. | ④>③>②>① | C. | ②>③>④>① | D. | ②>④>③>① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com