
(13��) ��1���������������������ҿ������������е��ʷ�Ӧ����:
6Ag(s) + O3(g) = 3Ag2O(s) ��H1
��֪2Ag2O(s) = 4Ag(s) + O2(g) ��H2
�����·�Ӧ: 2O3(g) = 3O2(g)�Ħ�H= ���æ�H1�ͦ�H2��ʾ��.
��2���ں�ѹ�£���CH4(g)��NO2(g)�����ܱ������з�����ѧ��Ӧ��
CH4(g) ��2NO2(g) N2(g) ��CO2(g) ��2H2O(g)
N2(g) ��CO2(g) ��2H2O(g)
�ڲ�ͬ�¶ȡ���ͬͶ�ϱ�ʱ��NO2��ƽ��ת���ʼ��±���
Ͷ�ϱ�[n(NO2) / n(CH4)] | 400 K | 500 K | 600 K |
1 | 60% | 43% | 28% |
2 | 45% | 33% | 20% |
��д���÷�Ӧƽ�ⳣ���ı���ʽK = ��
�����¶Ȳ��䣬���[n(NO2) / n(CH4)]Ͷ�ϱȣ���NO2��ƽ��ת���� �������������С�����䡱����
�����ϱ���֪�ÿ��淴Ӧ������Ӧ�� ��Ӧ��
��400 Kʱ����Ͷ�ϱ�Ϊ1��NO2��CH4�Ļ�����干0.04 mol������һװ�д����������У���ַ�Ӧ��ƽ��ʱNO2��������� ��
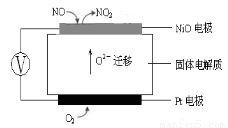
��3����ͼΪ�����Զ��������NOx����������̬�����ǵĹ���ԭ��ʾ��ͼ����NiO�缫��NO�����ĵ缫��ӦʽΪ�� ��
��1��2��H1+3��H2��2�֣�
��2���� ��3�֣� �ڼ�С ��2�֣� �� ���ȣ�2�֣�
��3�֣� �ڼ�С ��2�֣� �� ���ȣ�2�֣�
��17.4% ��2�֣�
��3��NO + O2����2e��= NO2 ��2�֣�
��������
�����������1����6Ag��s��+O3��g���T3Ag2O��s����H1����2Ag2O��s���T4Ag��s��+O2��g����H2�����ݸ�˹���ɿ�֪�١�2+�ڡ�3�ɵõ���2O3��g���T3O2��g������Ӧ�ȡ�H=2��H1+3��H2����2�����ں�ѹ�£���CH4��g����NO2��g�������ܱ������з�����ѧ��Ӧ��CH4��g��+2NO2��g��N2��g��+CO2��g��+2H2O��g������Ӧ��ƽ�ⳣ������ʽ������ƽ��״̬������Ũ���ݴη��˻����Է�Ӧ��Ũ���ݴη��˻����÷�Ӧ��ƽ�ⳣ���ı���ʽ K= �� �����¶Ȳ��䣬���[n��NO2��/n��CH4��]Ͷ�ϱȣ���NO2�����ʵ������ӣ�CH4��ƽ��ת��������NO2��ƽ��ת���ʼ�С����400Kʱ��Ͷ�ϱ�[n��NO2��/n��CH4��]=1��NO2��ƽ��ת����60%��500Kʱ��NO2��ƽ��ת����43%��˵���¶����ߣ�ƽ�������ƶ�����������ӦΪ���ȷ�Ӧ����400 Kʱ����Ͷ�ϱ�Ϊ1��NO2��CH4�Ļ�����干0.04 mol����������ת����Ϊ60%������һװ�д����������У���ַ�Ӧ����
�� �����¶Ȳ��䣬���[n��NO2��/n��CH4��]Ͷ�ϱȣ���NO2�����ʵ������ӣ�CH4��ƽ��ת��������NO2��ƽ��ת���ʼ�С����400Kʱ��Ͷ�ϱ�[n��NO2��/n��CH4��]=1��NO2��ƽ��ת����60%��500Kʱ��NO2��ƽ��ת����43%��˵���¶����ߣ�ƽ�������ƶ�����������ӦΪ���ȷ�Ӧ����400 Kʱ����Ͷ�ϱ�Ϊ1��NO2��CH4�Ļ�����干0.04 mol����������ת����Ϊ60%������һװ�д����������У���ַ�Ӧ����
CH4��g��+ 2NO2��g�� N2��g�� + CO2��g��+ 2H2O��g��
N2��g�� + CO2��g��+ 2H2O��g��
��ʼʱ�����ʵ��� 0.02 0.02 0 0 0
ת�������ʵ��� 0.006 0.02��0.6=0.012 0.006 0.006 0.012
ƽ��ʱ�����ʵ��� 0.014 0.008 0.006 0.006 0.012
ƽ��ʱNO2���������= ��
��
��3������NiO��һ������ʧ���Ӻ������ӷ�Ӧ���ɶ����������缫��ӦʽΪNO-2e-+O2-�TNO2��
���㣺�����˹���ɵ�Ӧ�á�ԭ��غ͵��أ���ѧƽ���Ӱ�����ء�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015�ӱ�ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
��6�֣��û���Ӧ��ͨʽ�ɱ�ʾΪ��
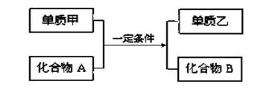
���ʼס��Һͻ�����A��BΪ��ѧ�������ʣ���ش��������⣺
��1����AΪ����Ԫ���γɳ����³�Һ̬�Ļ����������B����ɫ��Ӧ�ʻ�ɫ����÷�Ӧ�Ļ�ѧ����ʽΪ�� ��
��2��������һ�ֽ������ʣ��ڸ��������£�����Ӧ�����ں��Ӹֹ졣��÷�Ӧ�Ļ�ѧ����ʽΪ�� ��
��3�����������Ǻ�ɫ�ǽ������嵥�ʣ�������B��һ�ְ�ɫ�����������÷�Ӧ�Ļ�ѧ����ʽΪ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�ӱ�ʡ�����и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��N2(g)��3H2(g)  2NH3(g)��Ӧ�У���ʾ�÷�Ӧ����������
2NH3(g)��Ӧ�У���ʾ�÷�Ӧ����������
A��v��N2����0.1 mol����-1����-1 B��v��H2����0.9 mol����-1����-1
C��v��NH3����0.8 mol����-1����-1 D��v��N2����1 mol����-1��min-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡտ���и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и��������У�X���������ʣ�Y���������ʣ�Z��Ϊ��ȥ������Ҫ������Լ������������Լ���ȷ��һ����
X | Y | Z | |
A | NaHCO3��Һ | Na2CO3 | ͨ�������CO2 |
B | FeCl3��Һ | CuCl2 | Fe |
C | Fe2O3 | Al2O3 | ���� |
D | Na2SO4��Һ | Na2CO3 | BaCl2��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡտ���и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʵ���;��������Ϊ��;���������
A���������裨���ά�� B������裨�����оƬ��
C������þ���ͻ���ϣ� D��ˮ��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡտ���и߶���һѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
25��ʱ��10mL 0.1 mol��L��1NH4Cl��Һ�д���ƽ�⣺NH4+ +H2O NH3��H2O+H+�����ڸ�ƽ�⣬����������ȷ����
NH3��H2O+H+�����ڸ�ƽ�⣬����������ȷ����
A��c(H+) + c(NH4+) = c(Cl��) + c(OH��)
B�����뼸��Ũ���ᣬƽ�������ƶ�����Һ��pHֵ����
C���������ˮϡ��ʱ��ƽ�������ƶ�����Һ��c(H��)��С
D��c(NH4+) �� c(Cl��) �� c(H+) ��c(OH��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡտ���и߶���һѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��1.01��105Pa��298K�����£�2mol ������������ȼ������ˮ�����ų�484kJ�����������Ȼ�ѧ����ʽ��ȷ����
A��H2O(g) == H2(g) + 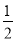 O2(g) ��H �� + 242kJ��mol-1
O2(g) ��H �� + 242kJ��mol-1
B��2H2(g) + O2(g) ==2H2O(l) ��H �� �� 484kJ��mol-1
C��H2(g) + 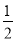 O2(g) ==H2O(g) ��H �� + 242kJ��mol-1
O2(g) ==H2O(g) ��H �� + 242kJ��mol-1
D��2H2(g) + O2(g) ==2H2O(g) ��H �� + 484kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и������������Ե�ˮ��Һ���ܴ����������
A��NH4+��Mg2����SO42����Cl�� B��Ba2����K����OH����NO3-
C��Al3����CH3COO����SO42����Cl�� D��Na����Ag����Cl����CO32-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�����з�һ�����У�߶���ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���л�ѧ��Ӧ��ʾ��ȷ����
A��Cl2ͨ��ˮ�У�Cl2+H2O=2H+ +Cl-+ClO-
B���ö��Ե缫��ⱥ��NaCl��Һ�� 2H++2Cl-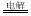 Cl2��+H2��
Cl2��+H2��
C����ʯī���缫���CuSO4��Һ��2Cu2++2H2O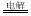 2Cu+O2��+4H+
2Cu+O2��+4H+
D����������������ʴʱ������ӦΪ��Fe - 3e- = Fe3+
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com