
【题目】乙二酸(HOOC—COOH)俗名草酸,是一种有还原性的有机弱酸,在化学上有广泛应用。
(1)小刚在做“研究温度对化学反应速率的影响”实验时,他往A、B两支试管中均加入4 mL 0.01 mol·L-1的酸性KMnO4溶液和2 mL 0.1 mol·L-1 H2C2O4(乙二酸)溶液,振荡,A试管置于热水中,B试管置于冷水中,记录溶液褪色所需的时间。褪色所需时间tA________tB(填“>”“=”或“<”)。已知该反应的离子方程式:2MnO![]() +5H2C2O4+6H+===10CO2↑+2Mn2++8H2O
+5H2C2O4+6H+===10CO2↑+2Mn2++8H2O
(2)实验室有一瓶混有泥沙的乙二酸样品,小刚利用上述反应的原理来测定其含量,具体操作为:
①配制250 mL溶液:准确称量5.000 g乙二酸样品,配成250 mL溶液。
②滴定:准确量取25.00 mL所配溶液于锥形瓶中,加少量酸酸化,将0.100 0 mol·L-1 KMnO4标准溶液装入______(填“酸式”或“碱式”)滴定管,进行滴定操作。
在滴定过程中发现,刚滴下少量KMnO4标准溶液时,溶液紫红色并没有马上褪去。将锥形瓶摇动一段时间后,紫红色才慢慢消失;再继续滴加时,紫红色就很快褪去,可能的原因是__________________________________________;判断滴定达到终点的现象是________________________________________________________________________。
③计算:重复上述操作2次,记录实验数据如下表。则消耗KMnO4标准溶液的平均体积为________ mL,此样品的纯度为____________。
序号 | 滴定前读数 | 滴定后读数 |
1 | 0.00 | 20.01 |
2 | 1.00 | 20.99 |
3 | 0.00 | 21.10 |
④误差下列操作会导致测定结果偏高的是________。
A.未用KMnO4标准溶液润洗滴定管
B.滴定前锥形瓶内有少量水
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D.观察读数时,滴定前仰视,滴定后俯视
【答案】酸式 < 反应生成的Mn2+对反应有催化作用 滴入最后一滴溶液,溶液由无色变成浅紫色,且半分钟内不褪色 20.00 90.00% AC
【解析】
(1)由于温度升高,化学反应速率加快,所以反应时间就越短,因此褪色所需时间tA<tB,故答案为:<;
(2)②KMnO4溶液有强氧化性,会腐蚀橡胶,所以KMnO4溶液应该装入酸式滴定管中,在实验中发现,刚滴下少量KMnO4溶液时,溶液迅速变成紫红色。将锥形瓶摇动一段时间后,紫红色慢慢消失;再继续滴加时,紫红色就很快褪色了可能的原因是反应中生成的Mn2+具有催化作用,所以随后褪色会加快;当滴入最后一滴酸性KMnO4溶液,锥形瓶中溶液从无色变为浅紫红色,且半分钟内不褪色,故答案为:酸式;反应生成的Mn2+对反应有催化作用;滴入最后一滴溶液,溶液由无色变成浅紫色,且半分钟内不褪色;
③分析3次实验的体积数据,可知:第三次误差太大,要舍去,消耗的KMnO4溶液的体积是V(KMnO4)=(20.10+19.90)ml÷2=20.00ml;n(KMnO4)=0.1000mol/L×0.020L=2×10-3mol;根据方程式可知n(H2C2O4)=5/2n(KMnO4)= 5/2×2×10-3mol=5×10-3mol,所以H2C2O4的质量是m=5×10-3mol ×90g/mol=0.45g,所以草酸的纯度是0.45g÷(5.000g÷10) × 100%=90.00%,故答案为:20.00;90.00%;
④A、未用标准浓度的酸性KMnO4溶液润洗滴定管,则标准溶液的浓度偏小,是消耗的体积偏大,则计算的草酸的物质的量偏大,正确;B、滴定前锥形瓶有少量水,不会产生任何影响,错误;C、滴定前滴定管尖嘴部分有气泡,滴定后气泡消失,则消耗的标准溶液体积偏大,所以计算的草酸的浓度就偏高,正确;D、观察读数时,滴定前仰视,滴定后俯视,则消耗的标准溶液体积偏小,所以是草酸溶液的浓度偏小,错误,故答案为:AC。


科目:高中化学 来源: 题型:
【题目】关于元素周期表的说法中正确的是( )
A. 元素周期表共7个周期、18个族B. 38号元素位于第五周期第IIA族
C. 非金属元素均位于周期表右侧D. 第六周期共计18种元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知分解1molKClO3放出热量38.8kJ,在MnO2下加热,KClO3的分解分为两步:
①2KClO3+4MnO2![]() 2KCl+2Mn2O7 慢
2KCl+2Mn2O7 慢
②2Mn2O7![]() 4MnO2+3O2 快
4MnO2+3O2 快
下列有关说法不正确的是
A. 1molKClO3所具有的总能量高于1molKCl所具有的总能量
B. 1gKClO3 ,1gMnO2,0.1gMn2O7混合加热,充分反应后MnO2质量仍为1g
C. KClO3分解速率快慢主要取决于反应①
D. 将固体二氧化锰碾碎,可加快KClO3的分解速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为元素在生物体内的含量分布情况,下列表述错误的是
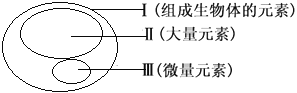
A. P、S、K、Ca、Zn属于大量元素
B. 在非生物界中都能找到,体现生物界与非生物界的统一性
C. Ⅱ和Ⅲ为生物体的必需元素,一旦缺乏就可能会导致相应的病症
D. Ⅲ含量虽少,却是生物体正常生命活动不可缺少的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2 L的密闭容器中通入气体X、Y、Z,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是

A. 该反应的化学方程式为2X+Y![]() 2Z
2Z
B. 反应开始至2min时,Z的平均反应速率为0.1 mol·L-1·min-1
C. 该反应为可逆反应
D. 4min时,X、Z的速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 溶液呈电中性,胶体带电荷。
B. 配制0.1 mol·L-1CuSO4溶液100 mL,称取1.6g硫酸铜晶体
C. 向饱和Ca(OH)2溶液中加入少量无水CaO固体,恢复原温度,溶液中Ca(OH)2的物质的量浓度不变
D. 制备Fe(OH)3胶体,可向沸水中滴加FeCl3饱和溶液并长时间煮沸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某市售盐酸试剂瓶标签上的部分信息如下:
盐酸
化学式:HCl
相对分子质量:36.5
密度约1.18 g·mL-1
HCl的质量分数:36.5%
(1)该盐酸中HCl的物质的量浓度=_____。
(2)取该盐酸50 mL加水稀释到100 mL,则稀释后溶液中c(HCl)=____。该实验选用的主要仪器有:烧杯、量筒、玻璃棒、和_________。
(3)该操作的正确顺序为_____(填序号)。
a.反复颠倒摇匀 b. 稀释浓盐酸c.用胶头滴管加水至刻度线 d.用量筒量取浓盐酸e.将配制好的溶液转入试剂瓶中贴上标签f.将溶液转入容量瓶
(4)下列情况对所配制的稀盐酸浓度有何影响?用“偏大”“偏小”或“无影响”填写。
a.所用的浓盐酸长时间放置在密封不好的容器中_____。
b.用量筒量取浓盐酸时,仰视刻度线_____。
c.洗涤量取过浓盐酸的量筒,并将洗液注入容量瓶中_____。
d.定容时俯视容量瓶的刻度线_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将2molA和2molB两种气体相混合后于容积为2L的某密闭容器中,发生如下反应3A(g) +B(g) ![]() xC(g) +2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g) +2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)x值等于_________;
(2)A的转化率为____________;
(3)生成D的反应速率为_________________;
(4)如果增大反应体系的压强,则平衡体系中C的质量分数_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com