
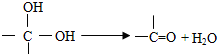
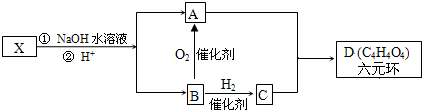
| 浓硫酸 |
| ℃170 |
| 高温、高压 |
| 催化剂 |
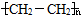 .
.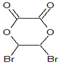 ,故A为HOOC-COOH,B为OHC-CHO,C为HOCH2CH2OH,A与B发生酯化反应反应生成环酯D为
,故A为HOOC-COOH,B为OHC-CHO,C为HOCH2CH2OH,A与B发生酯化反应反应生成环酯D为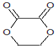 ,据此计算.
,据此计算. ,故A为HOOC-COOH,B为OHC-CHO,C为HOCH2CH2OH,A与B发生酯化反应反应生成环酯D为
,故A为HOOC-COOH,B为OHC-CHO,C为HOCH2CH2OH,A与B发生酯化反应反应生成环酯D为 ,
, ,所含官能团的名称为:酯基,故答案为:酯基;
,所含官能团的名称为:酯基,故答案为:酯基; ,含有酯基、溴原子,可以发生取代反应、消去反应,不能发生加成反应,故选:ab;
,含有酯基、溴原子,可以发生取代反应、消去反应,不能发生加成反应,故选:ab;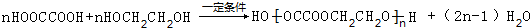 ,故答案为:
,故答案为: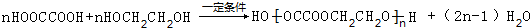 ;
; )有多种同分异构体,其中满足以下条件:a、能与NaHCO3溶液反应放出气泡,含有-COOH,b、能发生水解反应,含有酯基,c、分子内含有环状结构,符合条件的任意两种同分异构体的结构简式为:
)有多种同分异构体,其中满足以下条件:a、能与NaHCO3溶液反应放出气泡,含有-COOH,b、能发生水解反应,含有酯基,c、分子内含有环状结构,符合条件的任意两种同分异构体的结构简式为: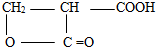 、
、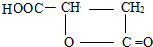 ,故答案为:
,故答案为: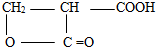 、
、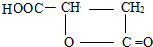 ;
;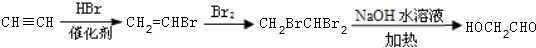 ,
,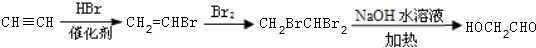 .
.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
| A、钠盐 | B、钾盐 | C、钙盐 | D、铁盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
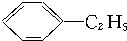 )的方法中,原子经济性最好的是(反应均在一定条件下进行)( )
)的方法中,原子经济性最好的是(反应均在一定条件下进行)( )A、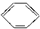 +C2H5Cl→ +C2H5Cl→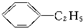 +HCl +HCl |
B、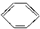 +C2H5OH→ +C2H5OH→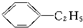 +H2O +H2O |
C、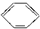 +CH2═CH2→ +CH2═CH2→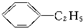 |
D、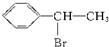 → →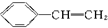 +HBr +HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 体积 | ||||
| 反应温度/℃ | 0.1mol?L-1Na2S2O3 | 0.1mol?L-1H2SO4 | H2O | |
| A | 10 | 10 | 10 | 0 |
| B | 10 | 9 | 10 | V1 |
| C | 50 | 8 | 10 | V2 |
| 实验步骤 | 预期现象及结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:
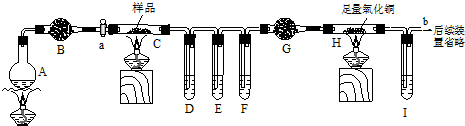
查看答案和解析>>
科目:高中化学 来源: 题型:
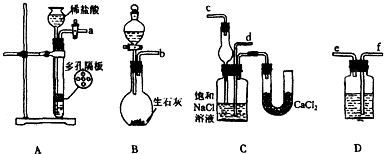
查看答案和解析>>
科目:高中化学 来源: 题型:
| 175℃ |
| △ |
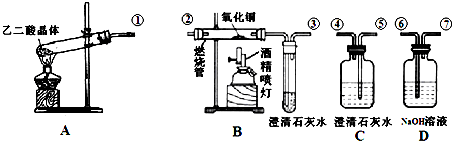
查看答案和解析>>
科目:高中化学 来源: 题型:
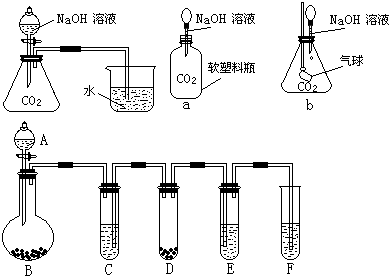
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| B、铁钉镀锌,将锌与电源负极相连,电镀过程需要控制电流强度、溶液pH等条件 |
| C、海轮外壳绑上锌板是采用牺牲阳极的阴极保护法,从而减缓钢铁腐蚀速率 |
| D、电解精炼铜时,阳极溶解铜的总质量和阴极析出铜的总质量相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com