
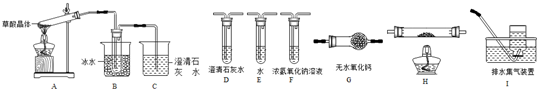
分析 (1)草酸晶体(H2C2O4•2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解,如果草酸受热分解,分解时会产生二氧化碳而使澄清石灰水变浑浊;草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水,B装置温度较低,有冷凝作用,防止干扰实验;
(2)①要检验生成CO,在甲组实验后,用浓氢氧化钠除去二氧化碳,用澄清石灰水检验二氧化碳,用碱石灰干燥CO,利用CO的还原性将CO氧化,再利用澄清石灰水检验生成的二氧化碳,用排水法收集CO;H装置中盛放的物质应该具有氧化性,且和CO反应有明显现象发生;
②CO具有还原性,其氧化产物是二氧化碳,二氧化碳能使澄清石灰水变浑浊;
(3)①要证明草酸酸性大于碳酸,可以利用强酸制取弱酸;
②利用酸碱中和滴定酸碱物质的量比确定草酸是二元酸.
解答 解:(1)草酸晶体(H2C2O4•2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解,如果草酸受热分解,分解时会产生二氧化碳,二氧化碳和氢氧化钙反应生成难溶性的碳酸钙沉淀而使澄清石灰水变浑浊,所以C中观察到的现象是:有气泡冒出且澄清石灰水变浑浊,说明有二氧化碳生成;草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水,草酸易挥发,导致生成的气体中含有草酸,草酸和氢氧化钙反应生成难溶性的草酸钙而干扰二氧化碳的检验,B装置温度较低,有冷凝作用,防止干扰二氧化碳的检验,
故答案为:有气泡冒出,澄清石灰水变浑浊;CO2;冷凝(水蒸气和草酸),防止草酸进入装置C反应生成沉淀而干扰CO2的检验;
(2)①要检验生成CO,在甲组实验后,用浓氢氧化钠除去二氧化碳,用澄清石灰水检验二氧化碳,用碱石灰干燥CO,利用CO和CuO发生还原反应生成CO2,再利用澄清石灰水检验生成的二氧化碳,用排水法收集CO避免环境污染,所以其连接顺序是A、B、F、D、G、H、D、I;
H装置中盛放的物质应该具有氧化性,且和CO反应有明显现象发生,CuO能被CO还原且反应过程中黑色固体变为红色,现象明显,所以H中盛放的物质是CuO,故答案为:F、D、G、H、D;CuO;
②CO具有还原性,其氧化产物是二氧化碳,二氧化碳能使澄清石灰水变浑浊,且CO将黑色的CuO还原为红色的Cu,只要H中黑色固体转化为红色且其后的D装置溶液变浑浊就说明含有CO,
故答案为:H中黑色粉末变为红色,其后的D中澄清石灰水变浑浊;
(3)①要证明草酸酸性大于碳酸,可以利用强酸制取弱酸,向盛有少量NaHCO3的试管里滴加草酸溶液,有气泡产生就说明草酸酸性大于碳酸,
故答案为:向盛有少量 NaHCO3的试管里滴加草酸溶液,有气泡产生就说明草酸酸性大于碳酸;
②草酸和NaOH发生中和反应时,如果草酸是二元酸,则参加反应的草酸物质的量应该是NaOH的一半,所以用NaOH标准溶液滴定草酸溶液,消耗NaOH的物质的量是草酸的2倍就说明草酸是二元酸,故答案为:用NaOH标准溶液滴定草酸溶液,消耗NaOH的物质的量是草酸的2倍.
点评 本题考查性质实验方案设计,侧重考查学生知识综合应用、实验基本操作能力及实验方案设计能力,综合性较强,难点是排列实验先后顺序,根据实验目的及物质的性质进行排列顺序,注意要排除其它因素干扰,难度较大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 油脂 | B. | 阿司匹林 | C. | 矿物质 | D. | 维生素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、H+、Fe2+、MnO4- | B. | Fe3+、Ba2+、SO42-、NO3- | ||
| C. | Al3+、Na+、SO42-、CO32- | D. | Fe3+、H+、SO42-、ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
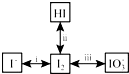
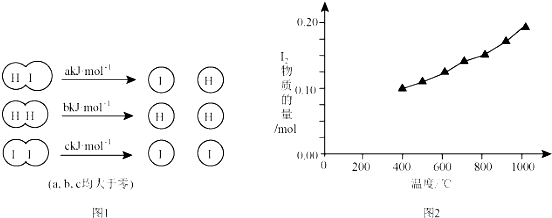
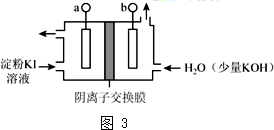
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
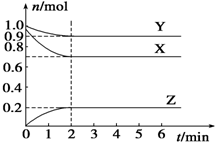 某温度时,在一个容积为2L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个容积为2L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
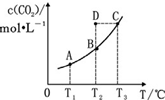 在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g).CO2(g)的平衡物质的量浓度 c(CO2)与温度 T 的关系如图所示.下列说法错误的是( )
在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g).CO2(g)的平衡物质的量浓度 c(CO2)与温度 T 的关系如图所示.下列说法错误的是( )| A. | 反应 CO(g)+H2O(g)?CO2(g)+H2(g)的△H>0 | |
| B. | 在 T2时,若反应处于状态 D,则有 v 正<v 逆 | |
| C. | 平衡状态 A 与 C 相比,平衡状态 A 的 c(CO)小 | |
| D. | 若 T1、T2时的平衡常数分别为 K1、K2,则 K1<K2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/℃ | 5 | 15 | 25 | 35 | 50 |
| K1 | 1100 | 841 | 680 | 533 | 409 |
| 起始浓度(mol/L) | 甲 | 乙 | 丙 |
| c(I2) | 0.1 | 0.2 | 0.2 |
| c(I-) | 0.2 | 0.1 | 0.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com