
| A. | 容器压强增大 | B. | 氧气浓度不变 | C. | KO2的量保持不变 | D. | 平衡常数增大 |
分析 对于反应4KO2(s)?2K2O(s)+3O2(g),达到平衡后,保持温度不变,缩小容器体积,相当于增大压强,平衡逆向移动,化学平衡常数只与温度有关,据此分析解答.
解答 解:A.缩小容器体积,相当于增大压强,平衡向逆反应方向移动,化学平衡常数=c(O2)3,温度不变,化学平衡常数不变,则氧气浓度不变,所以压强不变,故A错误;
B.化学平衡常数=c(O2)3,温度不变,化学平衡常数不变,则氧气浓度不变,故B正确;
C.平衡向逆反应方向移动,则KO2量增加,故C错误;
D.化学平衡常数只与温度有关,温度不变,平衡常数不变,故D错误;
故选B.
点评 本题考查了可逆反应平衡移动,根据压强与平衡移动方向之间的关系分析解答即可,注意平衡常数只与温度有关,与物质浓度无关,为易错点,题目难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称取28.6 g Na2CO3•10H2O,加入100 mL容量瓶中,加水溶解、定容 | |
| B. | 称取 28.6 g Na2CO3•10H2O,加入100 mL蒸馏水,搅拌、溶解 | |
| C. | 转移时将烧杯中溶液直接倒人容量瓶中 | |
| D. | 定容后,塞好瓶塞,反复倒转、摇匀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
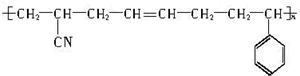 ,则合成该树脂的单体的种类和反应所属类型,正确的是( )
,则合成该树脂的单体的种类和反应所属类型,正确的是( )| A. | 1种,加聚反应 | B. | 2种,缩聚反应 | C. | 3种,加聚反应 | D. | 3种,缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 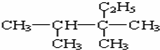 ,3,3-三甲基戊烷 ,3,3-三甲基戊烷 | B. | 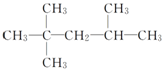 2,2,4三甲基戊烷 2,2,4三甲基戊烷 | ||
| C. | (CH3CH2)2CHCH3 3甲基戊烷 | D. | 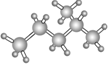 异戊烷 异戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1H2S水溶液中,H2S、HS-和S2-粒子数目之和为0.01NA | |
| B. | 0.16g氨基中含有N-H键的数目为0.02NA | |
| C. | 0.1mol CaO与0.2mol水完全反应后,溶液中Ca2+的数目为0.1NA | |
| D. | 2.24L氯气通入足量的NaOH溶液中,转移的电子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
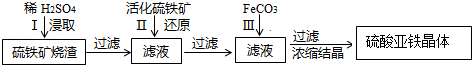
| pH | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 5.8 | 8.8 |
| Fe(OH)3 | 1.1 | 3.2 |
| Al(OH)3 | 3.0 | 5.0 |
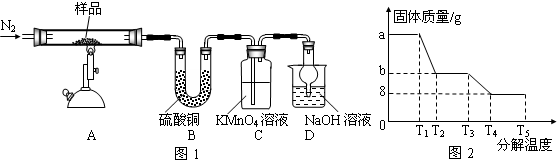
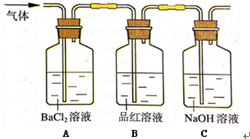 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com