
下列关于实验的误差分析错误的是
A、配制NaOH溶液时,用称量纸称取NaOH,所得溶液浓度偏低
B、用标准盐酸滴定未知浓度的NaOH溶液时,锥形瓶用NaOH溶液润洗,所得结果偏高
C、测定硫酸铜晶体中结晶水含量的过程中,不小心加热至固体呈微黑,所得结果偏高
D、测量气体摩尔体积时,镁条表面没有处理,所得结果偏高
科目:高中化学 来源: 题型:
X、Y、Z三种短周期元素,X元素的原子最外层只有一个电子,Y元素的原子M电子层的电子数为K、L上电子总数的一半, Z元素的原子L层电子数比Y原子L层电子数少2个,由这三种元素组成的化合物的化学式可能是( )。
A.X3YZ4 B.X2YZ3 C.XYZ2 D.X2YZ4
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组用如图装置探究氨的催化氧化。
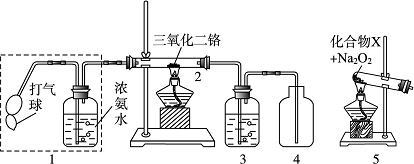
(1)氨催化氧化的化学方程式为______________________________________________。
(2)加热玻璃管2一段时间后,挤压1中打气球鼓入空气,观察到2中物质 呈红热状态;停止加热后仍能保持红热,该反应是________反应(填“
呈红热状态;停止加热后仍能保持红热,该反应是________反应(填“ 吸热”或“放热”)。
吸热”或“放热”)。
(3)为保证在装置4中观察到红棕色气体,装置3应装入________;若取消3,在4中仅观察到大量白烟,原因是_________________________________________________________。
(4)为实现氨的催化氧化,也可用装置5替换装置__ ______(填装置代号);化合物X为________(只写一种),Na2O2的作用是____________________________。
______(填装置代号);化合物X为________(只写一种),Na2O2的作用是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是
A、氢氧化钡溶液与稀硫酸混合:Ba2++SO42-→BaSO4↓
B、Fe与HCl反应:2Fe +6H+→ 2Fe3++3H2↑
C、氨水跟盐酸反应:OH-+H+→ H2O
D、醋酸与氢氧化钠溶液反应:CH3COOH+OH-→ CH3COO-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,针对表中元素,填写下列空白。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 |
| ① | ② | ③ | ④ | |||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑾ |
(1)⑦的阳离子结构示意图为______________。
(2)元素①和③形成的AB2型化合物中存在的化学键是________,该物质的电子式为_____。
(3)上述①~⑾元素中,金属性最强的元素是 (填元素符号),原子半径最小的元素是_____。(填元素符号)
(4)元素④ ⑩ ⑾的氢化物中稳定性最弱的是 (填化学式)。②⑧⑨的最高价氧化物对应水化物中酸性最强的是 。(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
空调中铝质蒸发器和冷凝器易氧化,影响空调器的寿命。铜-铝合金蒸发器和冷凝器的成功开发解决了制冷行业的一大难题,被称为二十一世纪制冷行业革命性的创新。
(1)为测定该铜-铝合金的质量分数,将5.6克合金样品粉碎,投入到足量盐酸中,充分反应后得到气体6.72L(标准状况)。此铜-铝合金中铝的质量分数为 (精确到0.01)。
(2)将上述反应液过滤,并将滤液稀释到100mL(写出简要计算过程)
①稀释后,溶液中Al3+的物质的量浓度为多少?
②从上述滤液中取出10mL,要想获得0.78克沉淀,至少加入0.5 mol/L NaOH溶液的体积为多少mL?
查看答案和解析>>
科目:高中化学 来源: 题型:
分析题目中的图表信息,根据信息完成填空。
Ⅰ.在恒温条件下将一定量X和Y的混合气体通入一容积为2 L的密闭容器中,X和Y两物质的浓度随时间变化情况如下图。
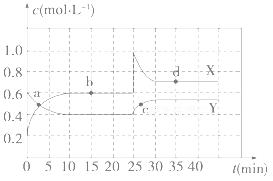
(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示):
_______________________________________________________。
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是________________。
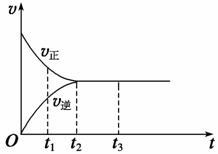 Ⅱ. (3)下图是可逆反应X2+3Y2
Ⅱ. (3)下图是可逆反应X2+3Y2  2Z在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是 。
2Z在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是 。
A.t1时,正反应速率大于逆反应速率;
B.t2时,反应达到限度;
C.t2~t3,反应不再发生;
D.t2~t3,各物质的浓度相等。
Ⅲ.以下是关于化学反应2SO2+O2  2SO3的两个素材:
2SO3的两个素材:
素材1:某温度和压强下2升容器中,不同时间点测得密闭体系中三种物质的物质的量。
|
| 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| SO2 | 1 | 0.7 | 0.5 | 0.35 | 0.2 | 0.1 | 0.1 | 0.1 |
| O2 | 0.5 | 0.35 | 0.25 | 0.18 | 0.1 | 0.05 | 0.05 | 0.05 |
| SO3 | 0 | 0.3 | 0.5 | 0.65 | 0.8 | 0.9 | 0.9 | 0.9 |
素材2:反应在不同条件下进行时SO2的转化率:
(SO2的转化率是反应的SO2占起始SO2的百分数,SO2的转化率越大,化学反应的限度越大)
|
| 0.1 MPa | 0.5 MPa | 1 MPa | 10 MPa |
| 400 ℃ | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 ℃ | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 ℃ | 73.7 | 85.8 | 90.0 | 96.4 |
根据以上的两个素材回答问题:
(4)根据素材1中计算20~30 s期间,用二氧化硫表示的化学反应平均速率为________。
(5)根据素材2中分析得到,提高该化学反应限度的途径有:
__________________________________________________________。
(6)根据素材1、素材2中分析得到,要实现素材1中SO2的转化率需控制的反应条件是
________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
验证淀粉水解可生成葡萄糖,进行了下列实验,该实验中操作步骤的排列顺序正确的是
①取少量淀粉加水制成溶液 ②加热煮沸 ③加入Cu(OH)2悬浊液 ④加入几滴稀硫酸 ⑤再加热 ⑥加入NaOH溶液,调PH至碱性
A.④②⑥③⑤ B.①⑤②⑥④③ C.①②④⑤③⑥ D.①④②⑥③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com