
| A. | 2NO(g)+O2(g)═2NO2(g) | |
| B. | Ba(OH)2•8H2O(s)+2NH4Cl(s)═BaCl2(aq)+2NH3•H2O(aq) | |
| C. | 2Na2O2(s)+2CO2(g)═2Na2CO3(s)+O2(g) | |
| D. | 2NO2(g)═N2O4(g) |
分析 一个化学反应能否自发进行,既与反应的焓变有关,又与反应的熵变有关,熵增加、放热有利于反应的自发进行,能够用焓判据判断反应自发进行的,该反应应为放热反应,据此解答.
解答 解:A.2NO(g)+O2(g)═2NO2(g),反应为熵减小的反应,能够自发进行是因为反应放热,故A不选;
B.Ba(OH)2•8H2O(s)+2NH4Cl(s)═BaCl2(aq)+2NH3•H2O(aq),反应为熵增加的、吸热的反应,反应能够自发进行是因为反应的熵增加,故B选;
C.2Na2O2(s)+2CO2(g)═2Na2CO3(s)+O2(g),反应为熵减小、放热的反应,反应能自发进行是因为反应放热,故C不选;
D.2NO2(g)═N2O4(g)为熵减小、放热反应,反应能自发进行是因为反应放热,故D不选;
故选:B.
点评 本题考查了反应自发进行的判断,明确反应能否自发进性既与熵变又与焓变有关,题目难度不大.


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 25℃时,HA的电离平衡常数KHA=$\frac{1}{9}$ | |
| B. | 0.01mol/LBOH溶液中阳离子浓度比c(B+):c(H+)=1010:1 | |
| C. | 0.01mol/L的两溶液中水得电离度α:α(HA)=α(BOH) | |
| D. | 溶液混合时,V1=V2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2+Ba(OH)2═BaO2+2H2O | |
| B. | Ag2O+H2O2═2Ag+O2↑+H2O | |
| C. | 2H2O2═2H2O+O2↑ | |
| D. | 3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 温度 物质的量 时间 | 2min | 4min | 6min | 8min | 10min | 12min |
| 450℃ | 0.2mol | 0.3mol | 0.35mol | 0.40mol | 0.50mol | 0.50mol |
| 480℃ | 0.25mol | 0.35mol | 0.45mol | 0.60mol | 0.60mol | 0.60mol |
| A. | 该反应是熵增,焓增的反应,在较高温度下能自发进行 | |
| B. | 恒温恒压,达到新平衡时,c(CO2)不变,c(MgCO3)增大 | |
| C. | 在2~8min之间CO2平均速率v(CO2)=$\frac{1}{30}$mol•L-1•min-1 | |
| D. | 升高温度,该反应平衡常数、分解速率和MgCO3分解率都增大. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、HCO3-、SO42-、H+ | B. | K+、AlO22-、H+、Cl- | ||
| C. | Fe2+、H+、Cl-、NO3- | D. | Al3+、H+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
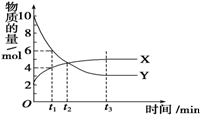 一定温度下在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图所示,下列叙述中错误的是( )
一定温度下在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图所示,下列叙述中错误的是( )| A. | 反应的化学方程式为7Y?3X | |
| B. | t1时,Y的浓度是X浓度的1.5倍 | |
| C. | t2时,反应达到平衡状态,正、逆反应速率相等 | |
| D. | t3时,反应达到平衡状态,逆反应速率等于正反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 盐酸滴入澄清石灰水中:Ca(OH)2+2H+═Ca2++2H2O | |
| C. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓ | |
| D. | 铜与硝酸银溶液反应:Cu+2Ag+═Cu2++2Ag |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com