
已知某温度下,反应SO2(g)+NO2(g)  SO3(g)+NO(g)的平衡常数K=0.24,下列说法正确的是( )
SO3(g)+NO(g)的平衡常数K=0.24,下列说法正确的是( )
A.该温度下反应2SO2(g)+2NO2(g)  2SO3(g)+2NO(g)的平衡常数为0.48
2SO3(g)+2NO(g)的平衡常数为0.48
B.若该反应ΔH<0,则升高温度化学平衡常数K减小
C.若升高温度,逆反应速率减小
D. 改变条件使平衡正向移动,则平衡时n(NO2)/n(NO)一定比原平衡小
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
一定条件下存在反应:CO(g)+H2O(g) CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界
CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界 没有热量交换) 密闭容器I、II、III,在I中充入1 mol CO和1 mol H2
没有热量交换) 密闭容器I、II、III,在I中充入1 mol CO和1 mol H2 O,在II中充入1 mol CO2 和1 mol H2,在III中充入2 mol CO 和2 mol H2O,700℃条件下开始反应。达到平衡
O,在II中充入1 mol CO2 和1 mol H2,在III中充入2 mol CO 和2 mol H2O,700℃条件下开始反应。达到平衡 时,下列说法正确的是( )
时,下列说法正确的是( )
A.容器I、II中正反应速率相同
B.容器I 、III中反应的平衡常数相同
、III中反应的平衡常数相同
C.容器I中CO 的物质的量比容器II中 的少
的少
D.容器I中CO 的转化率与容器II中CO2 的转化率之和小于1
查看答案和解析>>
科目:高中化学 来源: 题型:
亚氯酸钠(NaClO2)是重要漂白剂。探究小组开展如下实验,回答下列问题:
实验Ⅰ:制取NaClO2晶体:按下图装置进行制取。
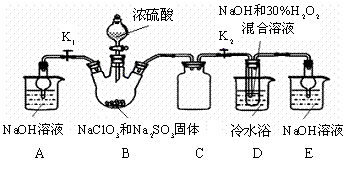 |
已知:NaClO2饱和溶液在低于38℃时析出NaClO2•3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
(1)用50%双氧水配制30%的H2O2溶液,需要的玻璃仪器除玻璃棒、胶头滴管、烧杯外,还需要 (填仪器名称);
(2)装置C的作用是 ;
(3)装置B内生成的ClO2气体与装置D中混合溶液反应生成NaClO2,生成NaClO2的反应方程式为 。
(4)如果撤去D中的冷水浴,可能导致产品中混有的杂质是 ;
(5)反应后,经以下步骤可从装置D的溶液获得NaClO2晶体。请补充完整操作iii。
i.55℃蒸发结晶; ii.趁热过滤; iii. ; iv.低于60℃干燥,得到成品。
实验Ⅱ:样品杂质分析与纯度测定
(6)上述实验制得的NaClO2晶体中含少量Na2SO4。产生Na2SO4最可能的原因是 ;
a. B中有SO2气体产生,并有部分进入D装置内
b. B中浓硫酸挥发进入D中与NaOH中和
c. B中的硫酸钠进入到D装置内
NaClO2中含少量Na2SO4可用重结晶的方法提纯。下列有关物质的提纯方案不正确的
是
| 被提纯的物质 [括号内物质是杂质] | 除杂试剂 | 除杂方法 | |
| a | CO(g) [CO2(g)] | NaOH溶液、 浓H2SO4 | 洗气 |
| b | NH4Cl(aq) [Fe3+(aq)] | NaOH溶液 | 过滤 |
| c | Cl2(g) [HCl(g)] | 饱和食盐水、浓H2SO4 | 洗气 |
| d | Na2CO3(s) [NaHCO3(s)] | — | 加热 |
(7)测定样品中NaClO2的纯度。测定时进行如下实验:
准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2-+ 4I-+4H+ =2H2O+2I2+Cl-,将所得混合液稀释成100mL待测溶液。
取25.00mL待测溶液,加入淀粉溶液做指示剂,用c mol·L-1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL(已知:I2 +2S2O32-=2I-+S4O62-)。
①确认滴定终点的现象是 ;
②所称取的样品中NaClO2的物质的量为 (用含c、V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验设计能够成功的是( )
A.检验亚硫酸钠试样是否变质:
试样 溶液
溶液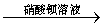 白色沉淀
白色沉淀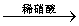 沉淀不溶解
沉淀不溶解
B.除去乙酸乙酯中混有的乙酸:
混合液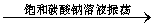 溶液分层
溶液分层 得上层液体
得上层液体
C.证明酸性条件下H2O2氧化性比I2强:
NaI溶液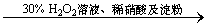 溶液变蓝色
溶液变蓝色
D.鉴定盐A的成分是FeBr2:
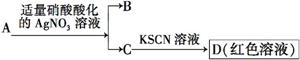
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验方案能达到预期目的的是( )
①实验室保存FeCl3溶液应加少量稀盐酸,并且放入少量的铁粉
②氢氧化钠溶液保存在配有橡胶塞的细口瓶中
③向溶液中滴入氯化钡溶液,再加稀硝酸能检验溶液中是否含有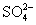
④用丁达尔效应可以区分食盐水和淀粉溶液
⑤工业上可用金属铝与V2O5在高温下冶炼矾,铝作还原剂
A.①②④ B.①②⑤
C.②④⑤ D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下2 L密闭容器中,3种气体起始状态和平衡状态时的物质的量(n)如下表所示。下列说法正确的是( )
| X | Y | W | |
| n(起始状态)/mol | 2 | 1 | 0 |
| n(平衡状态)/mol | 1 | 0.5 | 1.5 |
A.该温度下,此反应的平衡常数K=6.75
B.升高温度,若W的体积分数减小,则此反应ΔH>0
C.增大压强,正、逆反应速率均增大,平衡向正反应方向移动
D.该温度下,此反应的平衡常数表达式是
K=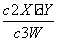
查看答案和解析>>
科目:高中化学 来源: 题型:
已知
Fe(s)+CO2(g) FeO(s)+CO(g) K1①
FeO(s)+CO(g) K1①
Fe(s)+H2O(g) FeO(s)+H2(g) K2②
FeO(s)+H2(g) K2②
H2(g)+CO2(g)  H2O(g)+CO(g) K3③
H2O(g)+CO(g) K3③
又已知不同温度下,K1、K2值如下:
| 温度/ ℃ | K1 | K2 |
| 500 | 1.00 | 3.15 |
| 700 | 1.47 | 2.26 |
| 900 | 2.40 | 1.60 |
(1)若500 ℃时进行反应①,CO2起始浓度为2 mol·L-1,2分钟后建立平衡,则CO2转化率为________,用CO表示的速率为_____________________________。
(2)900 ℃进行反应③,其平衡常数K3为________(求具体数值),焓变ΔH________0(填“>”“=”或“<”),若已知该反应仅在高温时正反应自发,则ΔS________0(填“>”“=”或“<”)。
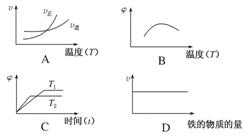
(3)下列图像符合反应②的是________(填序号)(图中v是速率,φ为混合物中H2的体积百分量)。
查看答案和解析>>
科目:高中化学 来源: 题型:
以溴乙烷为原料制备1,2-二溴乙烷,下列方案中最合理的是( )
A.CH3CH2Br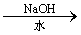 CH3CH2OH
CH3CH2OH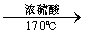 CH2=CH2
CH2=CH2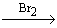 CH2BrCH2Br
CH2BrCH2Br
B.CH3CH2Br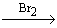 CH2BrCH2Br
CH2BrCH2Br
C.CH3CH2Br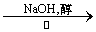 CH2=CH2
CH2=CH2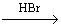 CH2BrCH3
CH2BrCH3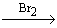 CH2BrCH2Br
CH2BrCH2Br
D.CH3CH2Br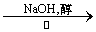 CH2=CH2
CH2=CH2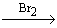 CH2BrCH2Br
CH2BrCH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
火力发电是通过化石燃料燃烧,使化石燃料中化学能转化为电能,其能量转化方式正确的是
A.化学能→电能 B.化学能→机械能→电能
C.化学能→热能→电能 D.化学能→热能→机械能→电能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com