
【题目】汽车尾气排放的NO和CO都是有毒的气体,科学家正在研究利用催化技术将尾气中的NO和CO转变成无毒的CO2和N2,减少污染。
(1)已知:N2(g)+O2(g)=2NO(g) △H=+180.0 kJ/mol
2C(s)+O2(g)=2CO(g) △H=-221.0 kJ/mol
2C(s)+2O2(g)=2CO2(g) △H=-787.0 kJ/mol
则尾气转化反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H= 。
N2(g)+2CO2(g) △H= 。
(2)对于反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g),为了测定在某种催化剂作用下的反应速率,用气体传感器测得不同时间的NO和CO浓度如下表
N2(g)+2CO2(g),为了测定在某种催化剂作用下的反应速率,用气体传感器测得不同时间的NO和CO浓度如下表
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/×10-4 mol/L | 3.00 | 2.25 | 1.75 | 1.36 | 1.00 | 1.00 |
c(CO)/×10-4 mol/L | 4.00 | 3.25 | 2.75 | 2.36 | 2.00 | 2.00 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
①前2s内的平均反应速率 υ(CO2)= mol/(Ls)。
②在该温度下,反应的平衡常数K= 。
(3)假设在恒容密闭容器中发生上述反应,下列有关说法正确的是 。
A.选用更有效的催化剂能提高尾气的转化率
B.升高反应体系的温度能提高反应速率, 提高尾气的转化率
C.相同温度下,若NO和CO的起始浓度分别为1.50×10-4 mol/L和2.00×10-4 mol/L,平衡时N2的体积分数比原平衡体系中N2的体积分数低
D.单位时间内消耗NO的物质的量等于生成CO2的物质的量时即达平衡状态

(4)用尾气NO2为原料可制新型硝化剂N2O5,原理:先将NO2转化为N2O
【答案】(1)-746.0 kJ/mol
(2)①6.25×10-5 ②104(3)C
(4)负 N2O4-2e— + 2HNO3 = 2N2O5 + 2H+ 不变
【解析】
试题分析:
(1)设3个热化学方程式的序数依次为①、②、③,依据盖斯定律③-②-①得到,反应的热化学方程式为:2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H=(-787 .0 kJ/mol)-(-221.0 kJ/mol)-(+180.0 kJ/mol)=-746.0 kJ/mol。
N2(g)+2CO2(g) △H=(-787 .0 kJ/mol)-(-221.0 kJ/mol)-(+180.0 kJ/mol)=-746.0 kJ/mol。
(2)①由表格中的数据可知2s内NO浓度的变化量为3.00×10-4-1.75×10-4=1.25×10-4mol/L,则υ(NO)=![]() =6.25×10-5mol/(Ls),由化学反应速率之比等于化学计量数之比,则υ(CO2)=υ(NO)=6.25×10-5mol/(Ls)。
=6.25×10-5mol/(Ls),由化学反应速率之比等于化学计量数之比,则υ(CO2)=υ(NO)=6.25×10-5mol/(Ls)。
②由表格中的数据可知到4s时达到化学平衡,则根据三段式:
2NO+2CO![]() 2CO2 +N2
2CO2 +N2
开始×10-4 3 4 0 0
转化×10-4 2 2 2 1
平衡×10-4 1 2 2 1
则K=![]() =
= ![]() =104,
=104,
(3)A.催化剂与转化率无关,故A错误;B.升高温度平衡向吸热反应方向移动,该反应正反应放热,平衡向逆反应方向移动,故B错误;C.由于是恒容容器,相同温度下,若NO和CO的起始浓度分别为1.50×10-4 mol/L和2.00×10-4 mol/L,则浓度相当于原平衡的一半,相当于减小压强,因该反应是气体系数减小的反应,减小压强,平衡逆向移动,所以平衡时N2的体积分数比原平衡体系中N2的体积分数低,故C正确;D.单位时间内消耗NO的物质的量等于生成CO2的物质的量是同一个方向的速率,不是正逆反应速率,故D错误;故选C。
(4)根据用NO2为原料制备N2O5的原理可知,NO2失去电子得到N2O5,可知电极X为阳极,则电源的a电极为正极,电源的b电极为负极。N2O4被氧化得N2O5,所以电解池中生成N2O5的电极反应式是N2O4+2HNO3-2e-=2N2O5+2H+,阳极产生的H+通过质子交换膜移到阴极再放电产生H2,所以溶液的pH无变化。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】质子数和中子数相同的原子A,其阳离子An+核外共有x个电子,则A的质量数为( )
A. 2(x-n) B. 2(x+n) C. 2x D. n+2x
查看答案和解析>>
科目:高中化学 来源: 题型:
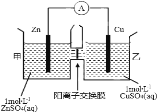
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过。下列有关叙述不正确的是
A.Zn电极上发生氧化反应
B.电子的流向为Zn→电流表→Cu
C.SO42-由乙池通过离子交换膜向甲池移动
D.电池工作一段时间后,乙池溶液的总质量明显增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 反应A(g)+3B(g)![]() 2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率
2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率
分别如下,其中反应速率最大的是( )
A.v(C)=0.04 mol/(L·s)
B.v(B)=0.06 mol/(L·min)
C.v(A)=0.15 mol/(L·min)
D.v(D)=0.01 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化石燃料的说法不正确的是
A.化石燃料的不完全燃烧是引起大气污染的主要原因之一
B.如果化石燃料能够完全燃烧就不会造成大气污染
C.燃料燃烧的产物CO2是一种温室气体
D.以液化石油气代替燃油可以减少大气污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验是进行科学探究的主要方法。回答下列问题:

(1)实验室利用A 发生装置制备的常见气体有_______________。
(2)检验装置B的气密性方法是______________。
(3)收集一瓶纯净氯气,选择上图装置,按气流方向,用小写字母表示连接顺序___________(装置不重复使用)。实验室检验氯气的方法是__________。
(4)某实验小组按顺序连接adcfeg制取并收集氨气,导致实验失败,原因是_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com