
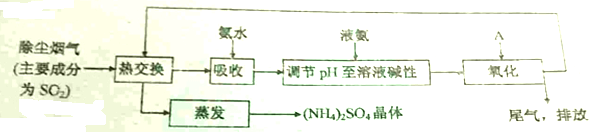
���� ����������Ҫ�ɷ�Ϊ����������������+4������л�ԭ�ԣ��ܱ����������������������Լ�A���ѡ��Ϊ�������������ǿ�������ɣ�ԭ�ϳ��㣬��ʹ�óɱ��ͣ����Ϲ�ҵ��������Ҫ�������Ƚ��������ڰ�ˮ���գ���ˮ�Ͷ�������Ӧ������������泥�ʹ��Һ������pH��NH3+HSO3-=NH4++SO32-������A��������������泥������Ƚ����������õ�����茶��壮
��1����������Ͱ�����ˮ��Ӧ����������李���������泥�
��2������pHʹ�õ��Լ�ΪҺ���������ʼ��ԣ�������������������ӷ�Ӧ�������Σ�
��3����ҵ����ԭ����ḻ����ʹ�óɱ�������������Ϊ���������ܽ�+4�۵���������+6�ۣ�
��4���������¶Ⱥܸߣ������Ƚ������ܼ���������Һ���������Һ�������ʣ�ͨ���Ƚ���������������ܣ��ﵽ���ܵ�Ч����
��5���������ο������ʣ�
��6����ú�е���S���Ϊ7%�������������������Ķ�������98%�����գ�������Ԫ���غ�n��SO2��=n[��NH4��2SO4��]���
��� �⣺����������Ҫ�ɷ�Ϊ����������������+4������л�ԭ�ԣ��ܱ����������������������Լ�A���ѡ��Ϊ�������������ǿ�������ɣ�ԭ�ϳ��㣬��ʹ�óɱ��ͣ����Ϲ�ҵ��������Ҫ�������Ƚ��������ڰ�ˮ���գ���ˮ�Ͷ�������Ӧ������������泥�ʹ��Һ������pH��NH3+HSO3-=NH4++SO32-������A��������������泥������Ƚ����������õ�����茶��壮
��1����������Ϊ�������������Ϊ�������壬���չ����п��ܷ�����2NH3+SO2+H2O=��NH4��2SO3��NH3+SO2+H2O=NH4HSO3���������չ����п��ܲ���������Ϊ����NH4��2SO3��NH4HSO3��
�ʴ�Ϊ����NH4��2SO3��NH4HSO3��
��2�������ʼ��ԣ�������������������ӷ�Ӧ��NH3+HSO3-=NH4++SO32-���ʴ�Ϊ��NH3+HSO3-=NH4++SO32-��
��3������A��������������泥���ѡ�����������������ǿ�������ɣ�ԭ�ϳ��㣬��ʹ�óɱ��ͣ����Ϲ�ҵ��������Ҫ��������Ϊ��������������狀�������Ӧ2��NH4��2SO3+O2=2��NH4��2SO4����������泥�
�ʴ�Ϊ��C��2��NH4��2SO3+O2=2��NH4��2SO4��
��4���������¶Ⱥܸߣ������Ƚ������ܼ���������Һ���������Һ�����ͺ����ʽᾧ��ͨ���Ƚ���������������ܣ�
�ʴ�Ϊ����Һ�������������ͺ����ʽᾧ�����ܣ�
��5�������Ϊ����Ԫ�ص��Σ�����ֲ�����ɵĻ��ʣ��ʴ�Ϊ�����ʣ�
��6����ú�е���S���Ϊ7%����������������ú10�ֿ���ȥ��������98%��SO2����ȥ�Ķ�����������ʵ���Ϊn��S��=n��SO2��=$\frac{10��1{0}^{6}��7%��98%g}{32g/mol}$��������Ԫ���غ�n��SO2��=n[��NH4��2SO4��]=$\frac{10��1{0}^{6}��7%��98%g}{32g/mol}$�������Ƶò�Ʒ=$\frac{10��1{0}^{6}��7%��98%g}{32g/mol}$��132g/mol��10-6t/g=2.83�֣��ʴ�Ϊ��2.83��
���� ���⿼�������е�SO2�Ĵ��������ն����������������ǽ����Ĺؼ����ϺõĿ���ѧ���������⡢��������������ע������غ�˼����6������Ŀ�Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
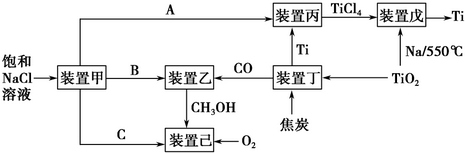
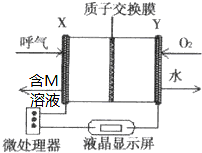 �鴦�ƺ��ʻ�����õġ���Яʽ�Ҵ������ǡ�����ȼ�ϵ��Ϊ����ԭ������ͼ�����缫���Ͼ�ΪPt���������Ҵ����Ա���ȫ����ΪCO2����ʵ���Ҵ�������ΪM������һ���缫�ķ�ӦʽΪ��CH3CH2OH-2e-��M+2H+������˵������ȷ���ǣ�������
�鴦�ƺ��ʻ�����õġ���Яʽ�Ҵ������ǡ�����ȼ�ϵ��Ϊ����ԭ������ͼ�����缫���Ͼ�ΪPt���������Ҵ����Ա���ȫ����ΪCO2����ʵ���Ҵ�������ΪM������һ���缫�ķ�ӦʽΪ��CH3CH2OH-2e-��M+2H+������˵������ȷ���ǣ�������| A�� | ����ڲ�H+��X���ƶ� | |
| B�� | ��һ��Y���ĵ缫��ӦʽΪ��O2+4e-+2H2O=4OH- | |
| C�� | �Ҵ���X���Ϸ�����ԭ��Ӧ�����Ӿ������·����Y�� | |
| D�� | ����ܷ�ӦΪ��2CH3CH2OH+O2��2CH3CHO+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
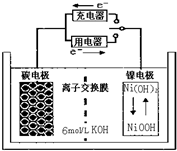
| A�� | ���ʱ̼�缫�Ϸ�����ԭ��Ӧ | |
| B�� | ���ʱNi�缫���Դ���������� | |
| C�� | �ŵ�ʱ̼�缫��ӦΪH2-2e-=2H+ | |
| D�� | �ŵ�ʱNi�缫��ӦΪNa��OH��+H2O+e-=Ni��OH��2+OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����������Ϊ���Ӿ��壮
����������Ϊ���Ӿ��壮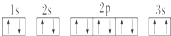 ����ͬѧ�����ĵ����Ų�ͼΥ��������ԭ����
����ͬѧ�����ĵ����Ų�ͼΥ��������ԭ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮ�м���NaCl��������캣ˮ�������ں���Ʒ�ij�;���� | |
| B�� | ������þ�ֽ�ʱ���մ��������������ӵ��ϳ���֬������ȼ�� | |
| C�� | �ƾ���ʹ�����ʱ��ԣ���ˮ�ƾ���ҽѧ�ϳ����������� | |
| D�� | ������ʳ��ƾ����˵��ۡ������ǡ��Ҵ��Ļ�ѧ�仯���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | ���� | �Լ� | ���� | |
| A | ���� | ��ϩ | ���Ը��������Һ | ϴ�� |
| B | �Ȼ�������Һ | �Ȼ��� | �������� | ���� |
| C | �� | �� | ����NaI��Һ | ��Һ |
| D | �������� | ���� | ����̼������Һ | ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
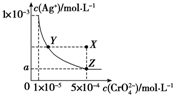
| A�� | T��ʱ����Y���Z�㣬Ag2CrO4��Ksp��� | |
| B�� | ��AgCrO4��Һ�м������K2CrO4����ʹ��Һ��Y���ΪX�� | |
| C�� | T��ʱ��Ag2CrO4��KspΪ1��10-8 | |
| D�� | ͼ��a=$\sqrt{2}$��10-4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶�/�� | 250 | 350 |
| K | 2.041 | x |
| c��CO��/mol•L-1 | c��H2��/mol•L-1 | c��CH3OH��/mol•L-1 | |
| 0min | 0.8mol•L-1 | 1.6mol•L-1 | 0 |
| 2min | 0.6mol•L-1 | y | 0.2mol•L-1 |
| 4min | 0.3mol•L-1 | 0.6mol•L-1 | 0.5mol•L-1 |
| 6min | 0.3mol•L-1 | 0.6mol•L-1 | 0.5mol•L-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com