
| A�� | �٢ڢۢ� | B�� | �ڢۢޢ� | C�� | �٢ۢޢ� | D�� | �٢ܢݢ� |
���� ����������������ʵ�����Ȼ����ݷ��Ӹ���N=nNA�����㣻
��NO2��N2O4�����ʽ��ΪNO2��
�ۻ��ý������������û���1molH2����Ԫ�صļ�̬��+1�۱�Ϊ0�ۣ�
�����28g���������ʵ�����Ȼ����ݵ����к�14��������������
��������Һ����HCl���ӣ�
��1molNa������O2��Ӧ���Ϊ+1�ۣ�
��һ���������������Ƕ�����������ľۼ��壻
�����1.06gNa2CO3�����ʵ�����Ȼ�����̼�����к�2����������������
��� �⣺�ٱ����22.4L�����������ʵ���Ϊ1mol���ʷ��Ӹ���N=nNA=NA��������ȷ��
��NO2��N2O4�����ʽ��ΪNO2����46g������к��е�NO2�����ʵ���Ϊ1mol����3NA��ԭ�ӣ�����ȷ��
�ۻ��ý������������û���1molH2����Ԫ�صļ�̬��+1�۱�Ϊ0�ۣ��ʵ�����1mol����ʱ�����2mol���ӣ������ʧȥ2mol���Ӽ�2NA��������ȷ��
��28g���������ʵ���Ϊ1mol���������к�14�����ӣ���1mol�����к�14NA�����ӣ��ʴ���
��HCl����ˮ����ȫ���룬��������Һ����HCl���ӣ��ʴ���
��1molNa������O2��Ӧ���Ϊ+1�ۣ���1mol�Ʒ�Ӧ��ʧȥNA�����ӣ��ʴ���
��һ���������������Ƕ�����������ľۼ��壬�ʺ�1mol���������Ľ����н����ĸ���С��NA�����ʴ���
��1.06gNa2CO3�����ʵ���Ϊ0.01mol����̼�����к�2�������ӣ���0.01mol̼�����к�0.02NA�������ӣ�����ȷ��
��ѡA��
���� ���⿼���˰���٤���������йؼ��㣬�ѶȲ���Ӧע�����չ�ʽ�����ú����ʵĽṹ��


 ��ͨ����ͬ����ϰ��ϵ�д�
��ͨ����ͬ����ϰ��ϵ�д� ����С����ͬ������ϵ�д�
����С����ͬ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ������ | K+��NH4+��Fe3+��Ba2+ |
| ������ | Cl-��CO32-��HCO3-��SO42- |
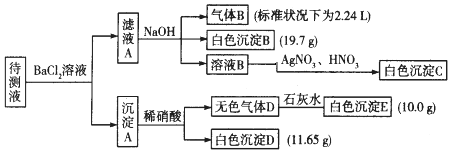
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ʯī���缫���AlC13��Һ��2Cl-+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$Cl2��+H2��+2OH- | |
| B�� | ���Ը��������Һ��H2O2��Һ��ϣ�2MnO4-+3H2O2+6H+�T2Mn2++4 O2��+6H2O | |
| C�� | ��NaHSO4��Һ�еμ�Ba��OH��2��Һ�����ٲ���������Ba2++OH-+H++SO42-�TBaSO4��+H2O | |
| D�� | ��Fe��NO3��2��NaBr�����Һ�еμ�ϡ���6Br -+2NO3-+8H+�T3Br2+2NO��+4H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ķ���Һϡ����ͬ��������Һ��pH���ۣ��ܣ��٣��� | |
| B�� | ���١��ܵ������ϣ�����Һ��PHΪ7 | |
| C�� | �ķ���Һ��ˮ�ĵ���̶��ɴ�С��˳��Ϊ���ۣ���=��=�� | |
| D�� | ���ڼ������ǡ����ȫ��Ӧ�����������Ϊ�ۣ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϴ�ӣ�2�� | B�� | ���ˣ�2�� | C�� | ��Һ��3�� | D�� | ���ˣ�3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| �� | �� | �� | �� | |
| ��ˮ | �������� | ���� | ���� | |
| pH | 11 | 11 | 3 | 3 |
| A�� | �ֱ��ˮϡ��10����������Һ��pHΪ���٣��ڣ��ۣ��� | |
| B�� | �¶�����10�棬������Һ��pH���� | |
| C�� | �ۢ��зֱ�����������Ȼ�������۵�pH��С���ܵ�pH���� | |
| D�� | ���٢�������Һ�������ϣ�������Һ��c ��C1-����c NH4+����c ��H+����c ��OH-�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com