
【题目】重水(D2O)是重要的核工业原料,下列说法错误的是( )
A.H2O与D2O互称同位素
B.氘
C.原子核外有1个电子
D.H与 D中子数不同
E.H218O与D216O的相对分子质量相同
科目:高中化学 来源: 题型:
【题目】室温下向10mLpH=3的醋酸溶液中加入水稀释后,下列说法正确是的
A.溶液中导电粒子的数目减少
B.溶液中![]() 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10mLpH=11的NaOH溶液,混合液的pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素可以形成多种化合物。回答下列问题:
(1)基态氮原子的价电子排布式是____;C、N、O 三种元素电负性从小到大的顺序是________。
(2)肼(N2H4)分子中氮原子轨道的杂化类型是______;肼可用作火箭燃料,燃烧时发生的反应时N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g) ΔH=11038.7kJ·mol-1,若该反应中8molN-H键断裂,则形成的σ键有____mol;肼能与硫酸反应生成N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4晶体内不存在______(填字母)。
A.离子键 B.共价键 C.配位键 D.范德华力
(3)氨是________(填“极性”或“非极性”)分子;氨的沸点高于膦(PH3)的原因是________。
(4)将氨气通入硫酸铜水溶液中形成[Cu(NH3)4]SO4深蓝色溶液,[Cu(NH3)4]SO4中阴离子的立体构型是______。
(5)单质铜和镍都是由金属键形成的晶体,元素铜和镍的第二电离能分别为:ICu=1959kJ·mol-1,INi=1753kJ·mol-1,ICu>INi的原因是_______。某镍白铜合金的立方晶胞结构如图所示。晶胞中镍原子与铜原子的个数比为_______。若合金的密度为dg/cm3,晶胞参数a=_________nm。
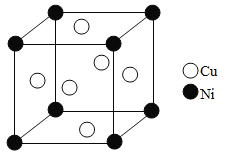
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe2O3俗称氧化铁红,常用作油漆等着色剂。某实验小组用部分氧化的FeSO4为原料,以萃取剂X(甲基异丁基甲酮)萃取法制取高纯氧化铁并进行铁含量的测定。实验过程中的主要操作步骤如下:
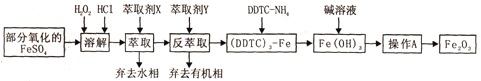
已知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮,当盐酸浓度降低时,该化合物解离。
② 3DDTC-NH4+Fe3+= (DDTC) 3-Fe↓+3NH4+
请回答下列问题:
(1)用萃取剂X萃取的步骤中,以下关于萃取分液操作的叙述中,正确的是____________。
A.FeSO4原料中含有的Ca2+、Cu2+等杂质离子几乎都在水相中
B.为提高萃取率和产品产量,实验时分多次萃取并合并萃取液
C.溶液中加入X,转移至分液漏斗中,塞上玻璃塞,如图用力振摇
D.振摇几次后需打开分液漏斗上口的玻璃塞放气
E.经几次振摇并放气后,手持分液漏斗静置待液体分层
F.分液时,将分液漏斗上的玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔,打开旋塞,待下层液体完全流尽时,关闭旋塞后再从上口倒出上层液体
(2)下列试剂中,可作反萃取的萃取剂Y最佳选择是_______________。
A.高纯水 B.盐酸 C.稀硫酸 D.酒精
(3)吸油量是反映氧化铁红表面性质的重要指标。吸油量大,说明氧化铁红表面积较大,则用在油漆中会造成油漆假稠,影响质量。不同浓度的两种碱溶液对产物吸油量影响如图所示,则上述实验过程中选用的碱溶液为_______________(填“NaOH”或“NH3·H2O”),反应的化学方程式为_________________。
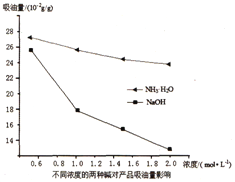
(4)操作A为______________________。
(5)现准确称取4.000g , 样品,经酸溶、还原为Fe2+,在容量瓶中配成100mL溶液,用移液管移取25.00 mL溶液于锥形瓶中,用0.l000mol/L的K2Cr2O7溶液进行滴定(还原产物是Cr3+),消耗K2Cr2O7溶液20.80mL。
① 用移液管从容量瓶中吸取25.00mL溶液后,把溶液转移到锥形瓶中的具体操作为_____。
② 产品中铁的含量为_______(假设杂质不与K2Cr2O7反应)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 足量Mg与2.8gN2完全反应后失去0.2NA电子
B. 3.0g由葡萄糖和冰醋酸组成的混合物中含有的原子总数为0.3NA
C. 常温常压下,2.8gC2H4含有共用电子对的数目为0.6NA
D. 16gO2含有NA个18O原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一体积可变的密闭容器中进行。改变下列条件能增大化学反应速率的是( )
CO(g)+H2(g)在一体积可变的密闭容器中进行。改变下列条件能增大化学反应速率的是( )
①增大C(s)的用量 ②将容器的体积缩小一半 ③保持体积不变,充入N2使容器内压强增大 ④保持压强不变,充入N2使容器体积增大 ⑤保持体积不变,充入水蒸气 ⑥升高温度
A. ②⑤⑥ B. ①②③⑥ C. ②③⑤⑥ D. ①②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项说法正确的是( )
A. “84”消毒液的有效成分是NaClO
B. SO2具有漂白性,可用于加工食品,使食品增白
C. 可以用酒精萃取碘水中碘单质
D. SO2气体通入Ba(NO3)2溶液中不能产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知将KI、盐酸、试剂X和淀粉四种溶液混合,无反应发生。若再加入双氧水,将发生反应H2O2+2H++2I-═2H2O+I2,且生成I2立即与试剂X反应而被消耗.一段时间后,试剂X将被反应生成I2完全消耗.由于溶液中I-继续被H2O2氧化,生成I2与淀粉作用,溶液立即变蓝.因此,根据试剂X量、滴入双氧水至溶液变蓝所需时间,即可推算反应H2O2+2H++2I-═2H2O+I2反应速率。下表为某同学依据上述原理设计的实验及实验记录(各实验均在室温条件下进行):
编号 | 往烧杯中加入的试剂及其用量(mL) | 催化剂 | 溶液开始变蓝时间(min) | ||||
0.1mol·L-1 KI溶液 | H2O | 0.01mol·L-1 X溶液 | 0.1mol·L-1 双氧水 | 0.1mol·L-1 稀盐酸 | |||
1 | 20.0 | 10.0 | 10.0 | 20.0 | 20.0 | 无 | 1.4 |
2 | 20.0 | m | 10.0 | 10.0 | n | 无 | 2.8 |
3 | 10.0 | 20.0 | 10.0 | 20.0 | 20.0 | 无 | 2.8 |
4 | 20.0 | 0 | 10.0 | 10.0 | 40.0 | 无 | t |
5 | 20.0 | 10.0 | 10.0 | 20.0 | 20.0 | 5滴Fe2(SO4)3 | 0.6 |
回答下列问题:
(1)已知:实验1、2的目的是探究H2O2浓度对H2O2+2H++2I-═2H2O+I2反应速率的影响。
实验2中m= ,n= 。
(2)一定温度下,H2O2+2H++2I-═2H2O+I2,反应速率可以表示为v=k·c a(H2O2)·c b (I-)·c(H+)(k为反应速率常数),则:
①实验4时,烧杯中溶液开始变蓝的时间t=__________min;
②根据上表数据可知,a、b的值依次为 和 。
(3)若要探究温度对H2O2+2H++2I-=2H2O+I2反应速率影响,在实验中温度不宜过高且采用水浴加热,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.π键是由两个p轨道“头碰头”重叠形成的
B.σ键就是单键,π键就是双键
C.乙烷分子中的键全为σ键,而乙烯分子中含σ键和π键
D.H2分子中含σ键,而Cl2分子中含π键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com