
����Ŀ����±���������ʽṹ��ѧ���о��ȵ㣬Ҳ����Ҫ�Ļ���ԭ�ϡ����Ȼ���(BCl3)��������ȡ������(B2H6)��Ҳ�����л��ϳɵĴ�����
�������ϣ���BCl3�ķе�Ϊ12.5 �棬�۵�Ϊ��107.3 �棻��2B��6HCl![]() 2BCl3����3H2���������������������ƣ�Ҳ��������������Һ��Ӧ��
2BCl3����3H2���������������������ƣ�Ҳ��������������Һ��Ӧ��
���ʵ�飺ijͬѧ�����ͼ��ʾװ�����������͵�����Ӧ�Ʊ����Ȼ���
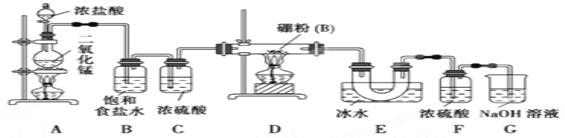
��ش��������⣺
��1���������ڱ���λ����__________________________��
��2��Eװ�õ�������___________________________�������ȥBװ�ã����ܵĺ����______________________��
��3��ʵ���п�����һ��ʢװ_____________(���Լ�����)�ĸ���ܴ���F��Gװ�ã�ʹʵ�����㡣
��4�����Ȼ�����ˮ���ҷ�Ӧ��������(H3BO3)�Ͱ�����д���÷�Ӧ�Ļ�ѧ����ʽ��______________��
��5��Ϊ��˳�����ʵ�飬��ȷ�IJ�����________(�����).
���ȵ�ȼA���ƾ��ƣ����ȼD���ƾ���
���ȵ�ȼD���ƾ��ƣ����ȼA���ƾ���
��ͬʱ��ȼA��D���ƾ���
��6�����㲹����������ļ���ʵ�飬����֤�ƵõIJ�Ʒ���Ƿ�����ۣ�ȡ������Ʒ���Թ��У��μ�Ũ________���ѧʽ����Һ���������ݲ���������Ʒ�к�����ۣ��������ݲ���������Ʒ������ۣ�д�������μ��Լ��Ļ�ѧ����ʽ___________________________��
���𰸡� �ڶ�������A�� ��ȴ���ռ����Ȼ��� ������Ȼ��ⷴӦ���ɲ���������������������������������壬������ը ��ʯ�� BCl3��3H2O=H3BO3��3HCl�� �� NaOH 2B+2NaOH+2H2O===2NaBO2+3H2��
��������A���������ڼ��������£��������̺�Ũ���ᷢ��������ԭ��Ӧ����Cl2����Ũ������лӷ��ԣ�ˮ������Ҳ�������������¶ȼӿ�Ũ����ӷ����ӿ�ˮ�������������ɵ�Cl2�к���HCl��H2O��B����ʳ��ˮ������Cl2��HCl��CŨ���������ˮ�ԣ�Ũ�����ܸ������壬�Ӷ��õ��ϴ�����Cl2����ֹ���ɵ�B��HCl��BCl3ˮ�⣻D���Ƶ�BCl3��Ȼ����E�õ�BCl3���壬Ϊ��ֹ���ɵ�BCl3ˮ���ҷ�ֹ������������F�������ò����G����δ��Ӧ��Cl2��
��1���������ڱ���λ���ǵڶ�������A�壻��2�����Ȼ���ķе�ͣ��ӷ�����Ҫ��ȴ��Ʒ��Bװ�õ�����������Cl2�л��е�HCl�����������֪�������Ȼ��ⷴӦ���ɵIJ����������������������������Ļ�����壬������ը����3��Fװ����������ˮ����������Gװ���е�ˮ��������U�ιܣ�Gװ�ÿ���ʢװ����������Һ����β������ʵ���п�����һ��ʢװ��ʯ�ҵĸ����������F+Gװ�ã���4�������������������ƣ�����Ļ�ѧʽΪH3BO3���������ᣨH3AlO3�������Ȼ�����ˮ���ҷ�Ӧ��������(H3BO3)�Ͱ�����д���÷�Ӧ�Ļ�ѧ����ʽ��BCl3��3H2O=H3BO3��3HCl�� ����5�����ȵ�ȼA���ƾ��ƣ�������װ���ж�����Cl2���ٵ�ȼD���ƾ��ƣ�ʹ֮������Ӧ���ʢ���ȷ�������ȵ�ȼD���ƾ��ƣ���ʱB����װ���еĿ���������Ӧ�õ�B2O3���ٵ�ȼA���ƾ���Ҳ���ܲ���BCl3�ˣ��ʢڴ���ͬʱ��ȼA��D���ƾ���Ҳ�ᵼ�²���B2O3��Ӱ���Ʊ�BCl3������ѡ�٣���6��B�������ԣ�ȡ������Ʒ���Թ��У��μ�ŨNaOH��Һ���������ݲ���������Ʒ�к�����ۣ��������ݲ���������Ʒ������ۣ������μ��Լ��Ļ�ѧ����ʽ2B+2NaOH+2H2O=2NaBO2+3H2��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������������˫��Ĥ���ҵ��۴�����ˮ�е�NH4+ �� ģ��װ����ͼ��ʾ������˵����ȷ���ǣ� �� 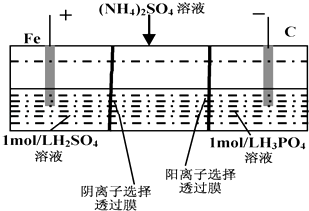
A.��������Һ����ɫ����ػ�ɫ
B.�����ĵ缫��ӦʽΪ��4OH����4e��=2H2O+O2��
C.���һ��ʱ�����������Һ�е����Լ���
D.���һ��ʱ�����������Һ�е�����һ���ǣ�NH4��3PO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڿ����о��õ���Ƭ5.0 gͶ��ʢ��500 mL 0.5 mol��L��1������Һ���ձ��У�����Ƭ�����ᷴӦ��������������v�뷴Ӧʱ��t������ͼ������������ʾ���������۴������(����)

A. O��a�β�������������Ϊ��������������������������Һ
B. b��c�β����������������ӽϿ����Ҫԭ��֮һ���¶�����
C. t>cʱ�������������ʽ�����Ҫ����Ϊ��Һ��c(H��)����
D. t��cʱ��Ӧ����ƽ��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�����÷���м(����������������������)������ʽ������[Fe(OH)SO4]��������������

��֪������������������������ʽ����ʱ��Һ��pH���±���
������ | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
��ʼ���� | 2.3 | 7.5 | 3.4 |
��ȫ���� | 3.2 | 9.7 | 4.4 |
�ش��������⣺
��1����ӦI��Һ�д��ڵĽ�����������___________________________��
��2����������NaHCO3��Ŀ���ǵ���pH��ʹ��Һ�е�________(����Fe3��������Fe2��������Al3����)�������ù�������������������������______________________��
��3����Ӧ�������ӷ���ʽΪ ____________________________����ʵ�������У���Ӧ����ͬʱͨ��O2�Լ���NaNO2��������O2��NaNO2�ڷ�Ӧ�о���______________�������뷴Ӧ��O2��11.2 L(��״��)�����൱�ڽ�ԼNaNO2�����ʵ���Ϊ________��
��4����ʽ����������ˮ�������Fe(OH)2�����ӣ��ɲ���ˮ������Fe2(OH)42���ۺ����ӡ���ˮ�ⷴӦ�����ӷ���ʽΪ____________________________��
��5����ҽҩ�ϳ����������������ᡢ����Ļ��Һ��Ӧ�Ʊ���ʽ�������������ҹ�����������Ʒ�в��ú���Fe2����NO3����Ϊ�������ò�Ʒ���Ƿ���Fe2����Ӧʹ�õ��Լ�Ϊ________(����ĸ)��
A. ��ˮ����B. KSCN��Һ����C. NaOH��Һ����D. ����KMnO4��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�������������;���ж�Ӧ��ϵ���� �� ��
A. Na2O2����CO2����O2��������������߹�����
B. ClO2���л�ԭ�ԣ�����������ˮ��ɱ������
C. Si����Ӳ�ȴ�����������ά
D. NH3������ˮ�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D��E���ֶ�����Ԫ�أ�Ԫ��A��һ��ԭ�������ӣ�Ԫ��B��C����2�����Ӳ㣬������������ɫ���������BC2 �� Ԫ��D���������Ӳ㣬����Ԫ��C����ͬһ���壬D��C�����д̼�����ζ������DC2��Ԫ��E��������E+�ĵ��Ӳ�ṹ��Ne�ĵ��Ӳ�ṹ��ͬ���Իش�
��1�����ǵ�Ԫ�������ǣ�ABCDE ��
��2��A��B�Ļ�����������ϣ�д��BA4�ĵ���ʽ��
C��E�Ļ�����������ϣ�д��E2C�ĵ���ʽ��
��3��A��B��C��E��ԭ�Ӱ뾶�Ӵ�С��˳��Ϊ��дԪ�ط��ţ���
��4��д��A��C�Ļ����A2C����C��E�Ļ����E2C2����Ӧ�Ļ�ѧ����ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����12mol/L������(��=1.19g/cm3)50mLϡ�ͳ�6mol/L������(��=1.10g/cm3)�����ˮ�����ԼΪ�� ��
A. 50mL B. 50.5mL C. 55mL D. 59.5mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ǧ������ɫ�������ڹŴ���������Ǧ���ʣ���Ǧ�ʡ��������ɴ˶�����
��1��ʹ���ִ���Ǧ�ʡ�д��ʱ����ֽ�����¡��ʻ�������Ч�ɷ���_________
��2������Ǧ��������ζ������ҽ�б���Ϊ��Ǧ�ǡ������о綾������ҩ����֪CH3COO��2Pb������ˮ������Ǧ������ƻ�Ϻ�Ӧ�����ӷ���ʽΪ��Pb2++2CH3COO-����CH3COO��2Pb���÷�Ӧ�ܹ���������Ҫԭ����_____________��
��3��Ǧ���γɶ��������
��Ǧ��������Pb3O4�ɿ�����2PbO��PbO2, Pb3O4��������ᷴӦ�Ļ�ѧ����ʽΪPb3O4+4HNO3��PbO2+2Pb(NO3)2+2H2O,��PbO2��_____����ᡱ������������������
��PbO�׳�����ɮ�����������ƶ��ּ������������������Һ��Ӧ���Ƶ�PbO2���÷�Ӧ�����ӷ���ʽΪ_________________________________��
��4��PbSO4��Ǧ���أ�����Pb- PbO2-H2SO4���е���Ҫ���ʣ�д�����ʱPbSO4����ԭΪijһ�缫���ϵĵ缫��Ӧʽ��_____________________________����������������96gʱ�������ϵ�·��ת�Ƶĵ�����Ϊ______NA����NAΪ����٤��������ֵ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com