
| A. | HCl | B. | BaCl2 | C. | AgNO3 | D. | NaOH |
 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:选择题
| A. | 100mL0.5mol/L MgCl2溶液 | B. | 200mL 0.25mol/L CaCl2溶液 | ||
| C. | 50mL 1.0mol/L NaCl溶液 | D. | 25mL0.4mol/L HCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4与Ba(OH)2溶液反应:Ba2++2OH-+2H+十SO42-→BaSO4↓+2H2O | |
| B. | CuSO4溶液与NaOH溶液反应:Cu2++2OH-→Cu(OH)2↓ | |
| C. | NaOH溶液中通入少量CO2:2OH-+CO2→CO32-+H2O | |
| D. | CH3COOH溶液与NaOH溶液反应:H++OH-→H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
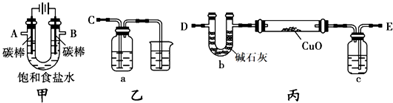
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | $\frac{1}{2}$H2SO4(aq)+$\frac{1}{2}$Ba(OH)2(aq)═$\frac{1}{2}$BaSO4(s)+H2O(l) | |
| B. | 2KOH(aq)+H2SO4(aq)═K2SO4(aq)+2H2O(l) | |
| C. | CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l) | |
| D. | NH3•H2O(aq)+HCl(aq)═NH4Cl(aq)+H2O(l) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同种原子 | B. | 同种元素 | ||
| C. | 互为同位素 | D. | 具有相同的核外电子排布 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com