
| A. | 溴离子具有氧化性 | B. | 溴单质是氧化剂 | ||
| C. | 该反应属于复分解反应 | D. | 氯元素的非金属性比溴元素强 |
分析 在氧化还原反应中得电子化合价降低的是氧化剂,失电子化合价升高的是还原剂,氧化剂具有氧化性,还原剂具有还原性,氧化剂对应的产物是还原产物,还原剂对应的产物是氧化产物,复分解反应是两种化合物相互交换成分生成另外的两种化合物,复分解反应一定不是氧化还原反应.
解答 解:A.该反应中溴离子失电子化合价升高,所以溴离子作还原剂,具有还原性,故A错误;
B.溴单质是氧化剂产物,故B错误;
C.该反应中有元素化合价的变化,属于氧化还原反应,复分解反应中反应前后各元素的化合价都不变,所以一定不属于复分解反应,故C错误;
D.根据氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性,所以氯气的氧化性比溴单质强,所以氯元素的非金属性比溴元素强,故D正确;
故选D.
点评 本题考查了基本概念和基本理论,根据元素化合价的变化来分析解答即可,难度不大.


科目:高中化学 来源: 题型:解答题
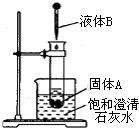 如图所示,把试管放入盛有25℃饱和石灰水的烧杯中,试管中开始放入固体试剂A,再在试管中用滴管滴入5mL液体试剂B.可见到烧杯中饱和的澄清石灰水变浑浊.试回答下列问题:
如图所示,把试管放入盛有25℃饱和石灰水的烧杯中,试管中开始放入固体试剂A,再在试管中用滴管滴入5mL液体试剂B.可见到烧杯中饱和的澄清石灰水变浑浊.试回答下列问题:| 固体试剂A | 液体试剂B | |
| ① | ||
| ② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氨作为清洁能源的反应原理是4NH3+5O2$→_{△}^{催化剂}$4NO+6H2O | |
| B. | 液氨可以作为溶剂使用,而氢的沸点极低,不易液化 | |
| C. | 氨气比空气轻,标准状况下密度约为0.76 g•L-1 | |
| D. | 氨气与氢气相比,优点在于氨气不容易发生爆炸,使用时更安全 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
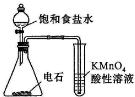
| A. | 用图装置检验乙炔的还原性 | |
| B. | 先加足量溴水,然后再加入酸性高锰酸钾溶液,鉴别己烯中是否混有少量甲苯 | |
| C. | 用裂化汽油从溴水中提取溴 | |
| D. | 将混合气体通过酸性高锰酸钾溶液,除去甲烷中混有的乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取少量卤代烃加入NaOH水溶液共热,冷却,再加入AgNO3溶液检验卤代烃中卤原子的存在 | |
| B. | 除去乙烷中混有乙烯,将混合气体通入酸性高锰酸钾溶液 | |
| C. | 用燃烧的方法鉴别甲烷与乙炔 | |
| D. | 用溴水鉴别苯和甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碱金属 | B. | 周期表右上角非金属元素 | ||
| C. | 金属与非金属分界线附近的元素 | D. | 过渡元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCH3COONa中含有的共用电子对总数为8NA | |
| B. | 标准状况下,将22.4LCl2溶于水,反应转移电子数为NA | |
| C. | 450℃时,在催化剂的作用下,将2molSO2与一定量的O2混合反应,一段时间后测得SO2消耗了$\frac{1}{2}$,则该正反应消耗了NA个SO2分子 | |
| D. | 78gNa2O2和Na2S的混合物中含有的阴离子数目一定是NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
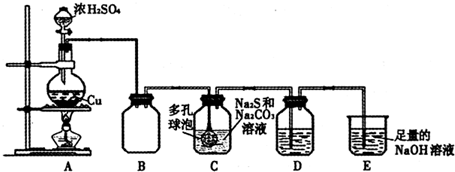
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com