
·ÖĪö øł¾Ż·“Ó¦Fe2++Ce4+ØTCe3++Fe3+£¬¼ĘĖćĻūŗÄCe£ØSO4£©2ČÜŅŗ21.00 mLĻūŗĵÄŃĒĢśĄė×ÓµÄĪļÖŹµÄĮ棬½ų¶ųµĆµ½100 mLČÜŅŗÖŠŃĒĢśĄė×ÓµÄĪļÖŹµÄĮ棬øł¾ŻĢśŌŖĖŲŹŲŗć£¬¼ĘĖć10ʬŅ©Ę¬ÖŠFeSO4•7H2Oŗ¬Į棬µĆµ½ĆæʬŅ©Ę¬ÖŠFeSO4•7H2Oŗ¬Į棬ŗĶ±źĒ©£ŗ0.3g/ʬ£¬FeSO4•7H2Oŗ¬ĮæĪŖ95%”«110%¶Ō±Č£¬µĆµ½“š°ø¼“æÉ£®
½ā“š ½ā£ŗøł¾Ż·“Ó¦Fe2++Ce4+ØTCe3++Fe3+£¬ĻūŗÄCe£ØSO4£©2ČÜŅŗ21.00 mLĻūŗĵÄŃĒĢśĄė×ÓµÄĪļÖŹµÄĮæŹĒ0.1000 mol•L-1”Į0.021L=0.0021mol£¬ĖłŅŌ100 mLČÜŅŗÖŠŃĒĢśĄė×ÓµÄĪļÖŹµÄĮæ5”Į0.0021mol=0.0105mol£¬øł¾ŻĢśŌŖĖŲŹŲŗć£¬10ʬŅ©Ę¬ÖŠFeSO4•7H2Oŗ¬ĮæŹĒ0.0105mol£¬ÖŹĮæŹĒ0.0105mol”Į278g/mol=2.919g£¬ĆæʬŅ©Ę¬ÖŠFeSO4•7H2Oŗ¬ĮæŹĒ0.2919£¼0.3g/ʬg£¬ĖłŅŌøĆ²¹ŃŖ¼Į²»ŗĻøń£¬“š£ŗøĆ²¹ŃŖ¼Į²»ŗĻøń£®
µćĘĄ ±¾Ģāæ¼²é»Æѧ·½³ĢŹ½µÄ¼ĘĖć£¬×¢ŅāׄהĢāÄæµÄŠÅĻ¢ŹĒ¹Ų¼ü£¬ÄѶČÖŠµČ£®


 Ź±æĢ×¼±ø×ÅŹī¼Ł×÷ŅµŌ×ÓÄܳö°ęÉēĻµĮŠ“š°ø
Ź±æĢ×¼±ø×ÅŹī¼Ł×÷ŅµŌ×ÓÄܳö°ęÉēĻµĮŠ“š°ø Źī¼ŁĻĪ½Ó½Ģ²ÄĘŚÄ©Źī¼ŁŌ¤Ļ°Īäŗŗ³ö°ęÉēĻµĮŠ“š°ø
Źī¼ŁĻĪ½Ó½Ģ²ÄĘŚÄ©Źī¼ŁŌ¤Ļ°Īäŗŗ³ö°ęÉēĻµĮŠ“š°ø ¼ŁĘŚ×÷ŅµŹī¼Ł³É³¤ĄÖŌ°ŠĀ½®ĒąÉŁÄź³ö°ęÉēĻµĮŠ“š°ø
¼ŁĘŚ×÷ŅµŹī¼Ł³É³¤ĄÖŌ°ŠĀ½®ĒąÉŁÄź³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| X | ||
| M | Y | |
| Z | N |
| A£® | ŌŖĖŲYÓėŌŖĖŲZµÄ×īøßÕż»ÆŗĻ¼ŪÖ®ŗĶµÄŹżÖµµČÓŚ13 | |
| B£® | ŌŖĖŲZµÄŗ¬ŃõĖįµÄĖįŠŌ±ČŌŖĖŲNµÄĒæ | |
| C£® | Ąė×Ó°ė¾¶µÄ“óŠ”Ė³ŠņĪŖZ£Øn+1£©-£¾M£Øn+1£©-£¾Yn- | |
| D£® | ZµÄĘųĢ¬Ēā»ÆĪļµÄ»¹ŌŠŌŗĶČČĪČ¶ØŠŌ¾ł±ČNĒæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĘÆ°×·Ū±£“ęŌŚĆܱÕČŻĘ÷ÖŠ | B£® | ŠĀÖĘĀČĖ®±£“ęŌŚ×ŲÉ«ĘæÖŠ | ||
| C£® | AgBr±£“ęŌŚĘÕĶز£Į§ŹŌ¼ĮĘæÖŠ | D£® | ĶłŅŗäåÖŠ¼ÓÉŁĮæĖ®²¢ĆÜ·ā±£“ę |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 13.6g | B£® | 10.2g | C£® | 6.8g | D£® | 1.7g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 Ņ»¶ØĪĀ¶ČĻĀ£¬½«0.4mol SO2ŗĶ0.2mol O2·ÅČė¹Ģ¶ØČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©”÷H=-196.6kJ/mol£¬·“Ó¦ÖŠSO3µÄĪļÖŹµÄĮæÅØ¶ČµÄ±ä»ÆĒéæöČēĶ¼£ŗ
Ņ»¶ØĪĀ¶ČĻĀ£¬½«0.4mol SO2ŗĶ0.2mol O2·ÅČė¹Ģ¶ØČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©”÷H=-196.6kJ/mol£¬·“Ó¦ÖŠSO3µÄĪļÖŹµÄĮæÅØ¶ČµÄ±ä»ÆĒéæöČēĶ¼£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ²Ł ×÷ | ĻÖ Ļó |
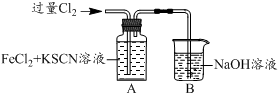 | I£®AÖŠČÜŅŗ±äŗģ II£®ÉŌŗó£¬ČÜŅŗÓÉŗģÉ«±äĪŖ»ĘÉ« |
 £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com