
下列鉴别方法或除杂可行的是( )
A.用新制的氢氧化铜鉴别乙醛、甲酸、乙酸、己烯
B.用溴水鉴别乙醇、苯、环己烯、苯酚,甲苯
C.除去苯中混有的苯酚,加入溴水后过滤
D.检验丙烯醛(CH2=CHCHO)中的醛基,加入溴水,若溴水褪色,则证明含有醛基
科目:高中化学 来源:2015届浙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
下列排序正确的是
A.酸性:H3AsO4> H2SO4>H3PO4 B.碱性:Ba(OH)2<Ca(OH)2<KOH
C.熔点:MgBr2<SiCl4<SiC D.沸点:PH3<NH3<H2O
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高二下学期第一次质量检测化学试卷(解析版) 题型:实验题
某化学小组以苯甲酸为原料,制取苯甲酸甲酯。已知有关物质的沸点如下表:
物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
沸点/℃ | 64.7 | 249 | 199.6 |
Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入12.2g苯甲酸和20ml甲醇(密度约0.79g·mL-1 ),再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。‘
(1)浓硫酸的作用是 ;
 简述混合液体时最后加入浓硫酸的理由: 。
简述混合液体时最后加入浓硫酸的理由: 。
(2)甲、乙、丙三位同学分别设计了如下图三套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。根据有机物的沸点,最好采用 装置(填“甲”或“乙”或“丙”)。

Ⅱ.粗产品的精制
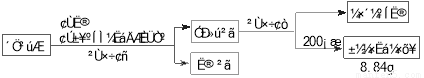
(3)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用下列流程进行精制,请根据流程图写出操作方法的名称。操作Ⅰ 操作Ⅱ 。
(4)能否用NaOH溶液代替饱和碳酸钠溶液? (填“能”或“否”),
并简述原因 。
(5)通过计算,苯甲酸甲酯的产率是 。
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高二下学期第一次质量检测化学试卷(解析版) 题型:选择题
下列关系正确的是( )
A.熔点:戊烷>2,2一二甲基戊烷>2,3一二甲基丁烷>丙烷
B.密度:CCl4>CHCl3>H2O>苯
C.同质量的物质燃烧耗O2量:丙炔>乙烷>乙烯>乙炔>甲烷
D.同物质的量物质燃烧耗O2量:已烷>环已烷>苯>苯甲酸
查看答案和解析>>
科目:高中化学 来源:2015届河南许昌市五校高二下学期第一次联考化学试卷(解析版) 题型:实验题
某同学用下列装置(固定、加热仪器和橡胶管已经省略)进行有关气体制取及其相关实验的探究,回答下列问题.

(1)若用装置①制取NH3,其反应的化学方程式为 ;多余的氨气应选用 装置吸收。(填装置序号,下同)
(2)若用装置②制乙炔,其反应的化学方程式为 ;要测定生成乙炔的体积,则必须选择的装置是 ,因制取的乙炔常含有杂质,若要除去杂质,所选装置中应盛放的试剂为: 。
(3)若用装置②制取乙烯,少了一种重要仪器 _。
(4)若用0.01mol/L的酸性高锰酸钾溶液滴定未知浓度的草酸溶液,酸性高锰酸钾溶液应装在装置 中。
查看答案和解析>>
科目:高中化学 来源:2015届河南许昌市五校高二下学期第一次联考化学试卷(解析版) 题型:选择题
已知2SO2(g)+O2(g)  2SO3 (g) △H =-a kJ·mol-1(a>0)。恒温恒容下,在10L的密闭容器中加入0.1molSO2和0.05molO2,经过2min达到平衡状态,反应放出热量x kJ
2SO3 (g) △H =-a kJ·mol-1(a>0)。恒温恒容下,在10L的密闭容器中加入0.1molSO2和0.05molO2,经过2min达到平衡状态,反应放出热量x kJ
下列判断正确的是( )
A.反应放出热量x=0.05 a
B.反应达到平衡状态时,2v (SO2) 消耗= v (O2) 生成
C.若恒温恒压下,在10L的密闭容器中加入0.1molSO2和0.05molO2,平衡后反应放出的热量y kJ,则y < x
D.升高温度,平衡常数变小
查看答案和解析>>
科目:高中化学 来源:2015届河南许昌市五校高二下学期第一次联考化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗数,下列叙述正确的是( )
A. 7.8gNa2O2固体中阴、阳离子数之和一定为0.3NA
B. 室温下,14.0g乙烯和丁烯的混合气体中含有的氢原子数目为NA
C.0.1mol Fe在0.1mol Cl2中充分燃烧,转移的电子数为0.3NA
D.常温常压下,1mol甲基所含的电子总数为7 NA
查看答案和解析>>
科目:高中化学 来源:2015届河南省洛阳市高二上学期期末检测化学试卷(A)(解析版) 题型:选择题
反应CO(g)+NO2(g)  CO2(g)+NO(g) ΔH<0,在温度t1时达到平衡,c1(CO)=c1(NO2)=1.0 mol·L-1,其平衡常数为K1。其他条件不变,升高反应体系的温度至t2时,反应物的平衡浓度分别为c2(CO)和c2(NO2),平衡常数为K2,则
CO2(g)+NO(g) ΔH<0,在温度t1时达到平衡,c1(CO)=c1(NO2)=1.0 mol·L-1,其平衡常数为K1。其他条件不变,升高反应体系的温度至t2时,反应物的平衡浓度分别为c2(CO)和c2(NO2),平衡常数为K2,则
A.若增大CO浓度,K2 和K1都增大 B.K2 >K1
C.c2(CO)=c2(NO2) D.c1(CO)>c2(CO)
查看答案和解析>>
科目:高中化学 来源:2015届河北省高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列有关化学实验操作正确的是 _(填序号)
①实验室进行石油的分馏实验时,温度计水银球插入石油液面以下
②由于碘在乙醇中的溶解度较大,用乙醇萃取分离溶于水中的碘。
③验证RX是碘代烷,把RX与烧碱水溶液混合加热后,将溶液冷却后再加入硝酸银溶液。
④实验室用无水乙醇和浓硫酸共热制乙烯时,把温度计水银球插入液面以下。
⑤分离苯和苯酚的混合液,先加入适量浓溴水,再过滤、分液,即可实现。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com