
2.8 g Fe全部溶于一定浓度、200 mL 的HNO3溶液中,得到标准状况下的气体1.12 L,测得反应后溶液的pH为1。若反应前后溶液体积变化忽略不计,则下列有关判断正确的是 ( )。
A.反应后溶液中c(NO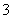 )=0.80 mol·L-1
)=0.80 mol·L-1
B.反应后的溶液最多还能溶解1.82 g Fe
C.反应前HNO3溶液的浓度为1.0 mol·L-1
D.1.12 L气体是NO、NO2的混合气体
解析 据题意,硝酸过量:0.2 L×0.1 mol·L-1=0.02 mol,反应生成Fe3+:2.8 g÷56 g·mol-1=0.05 mol,据反应后溶液中的电荷守恒,得c(NO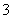 )=(0.05 mol×3+0.02 mol×1)÷0.2 L=0.85 mol·L-1,故A项错误;反应后的溶液与铁发生反应的离子方程式为:
)=(0.05 mol×3+0.02 mol×1)÷0.2 L=0.85 mol·L-1,故A项错误;反应后的溶液与铁发生反应的离子方程式为:
3Fe + 8H++2NO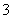 ===3Fe2++2NO↑+4H2O
===3Fe2++2NO↑+4H2O
0.02 mol×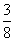 0.02 mol
0.02 mol
2Fe3+ + Fe === 3Fe2+
0.05 mol 0.025 mol
则最多能溶解铁:(0.02 mol×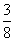 +0.025 mol)×56 g·mol-1=1.82 g,故B项正确;据氮原子守恒,反应前HNO3溶液的浓度为0.05 mol×3+0.02 mol+1.12 L÷22.4 L·mol-1)÷0.2 L=1.1 mol·L-1,故C项错误;2.8 g Fe生成Fe3+失去电子的物质的量为0.15 mol,根据得失电子守恒,1.12 L即0.05 mol气体得到电子的物质的量为0.15 mol,1.12 L气体应是NO气体,故D项错误。
+0.025 mol)×56 g·mol-1=1.82 g,故B项正确;据氮原子守恒,反应前HNO3溶液的浓度为0.05 mol×3+0.02 mol+1.12 L÷22.4 L·mol-1)÷0.2 L=1.1 mol·L-1,故C项错误;2.8 g Fe生成Fe3+失去电子的物质的量为0.15 mol,根据得失电子守恒,1.12 L即0.05 mol气体得到电子的物质的量为0.15 mol,1.12 L气体应是NO气体,故D项错误。
答案 B


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列说法正确的是( )
A.酸和醇反应一定能生成酯,且酯化反应是可逆反应
B.实验证实 可使Br2/CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳
可使Br2/CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳
双键
C.DDT的结构简式为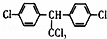 ,分子中最多有14个碳原子共平面
,分子中最多有14个碳原子共平面
D.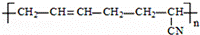 的单体是CH3﹣C≡C﹣CH3和CH2=CH﹣CN
的单体是CH3﹣C≡C﹣CH3和CH2=CH﹣CN
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )。
①氯气的性质活泼,它与氢气混合后立即发生爆炸 ②实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钙溶液吸收 ③新制氯水的氧化性强于久置氯水的氧化性 ④检验HCl气体中是否混有Cl2,方法是将气体通入硝酸银溶液 ⑤除去HCl气体中的Cl2,可将气体通入饱和食盐水中
A.①②③ B.②③④
C.③ D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+浓度和加入铁粉的物质的量之间的关系如下图所示。则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为 ( )。

A.1∶1∶1 B.1∶3∶1
C.3∶3∶8 D.1∶1∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
往100 mL的NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M。通入的CO2的体积V(标准状况)与M的质量(W)的关系如图所示。
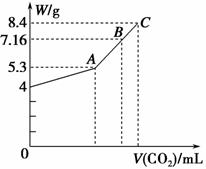
试解答下列问题:
(1)A点时,白色固体M的化学式为________,通入标准状况下的CO2的体积为________ mL。
(2)C点时,白色固体M的化学式为________,通入标准状况下的CO2的体积为________ mL。
(3)B点时M的组成成分为________(用化学式表示),通入的标准状况下的CO2的体积为________ mL。
(4)该NaOH溶液的物质的量浓度为________。
(5)如何检验B点溶液中的阴离子?
查看答案和解析>>
科目:高中化学 来源: 题型:
氢化亚铜(CuH)是一种不稳定的物质,能在氯气中燃烧,也能与酸反应。用CuSO4溶液和“某物质”在40~50 ℃时反应可生成CuH。下列叙述中错误的是 ( )。
A.“某物质”具有还原性
B.CuH与盐酸反应可能产生H2
C.CuH与足量稀硝酸反应:CuH+3H++NO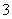 ===Cu2++NO↑+2H2O
===Cu2++NO↑+2H2O
D.CuH在氯气中燃烧:CuH+Cl2===CuCl+HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
Fe3O4是重要的化学试剂,铁粉在氧气中燃烧是制取它最为常见和快捷的方法。图1是制取四氧化三铁的系列装置,A装置用于制取二氧化碳气体,并要求气流稳定,流速可控。
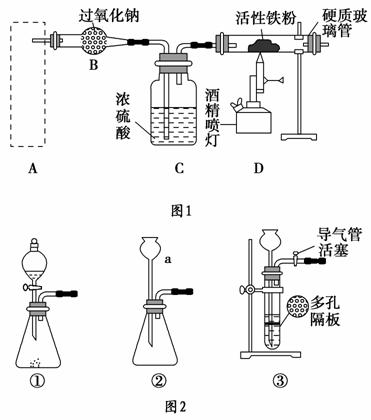
请回答下列问题:
(1)图2中仪器a的名称是________。
(2)根据题目要求,在图2中最好选择________(填序号)作为A装置。
(3)对图2中装置①进行气密性检查的方法是________,向分液漏斗中加足量水,过一会,水不再下滴,说明装置①的气密性良好。
(4)在B装置中发生的主要反应的化学方程式是_________________________ _______________________________________________________________________________________________________________________。
(5)当产生的气体与事先预热的铁粉接触时,在硬质玻璃管中将观察到的明显现象是________________________________________________________。
(6)反应一段时间后,若将硬质玻璃管中的固体粉末用盐酸溶解,取少许溶液于试管中,加入淀粉碘化钾溶液,没有蓝色出现,推测固体粉末中除Fe3O4外,一定有_______________________________________________________。
(7)若铁粉被完全消耗,某同学为确定生成物中有+2价铁,取少量生成物于试管中,加入适量的稀硫酸溶解。
①写出溶解过程发生反应的离子方程式______________________ ________________________________________________________。
②写出确定+2价铁所用试剂名称、操作步骤、实验现象和结论_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机化学发展史的说法错误的是( )
A.中国科学家成功合成了结晶牛胰岛素,标志着人类合成蛋白质时代的开始
B.德国化学家李比希提出运用同位素示踪法研究化学反应历程
C.瑞典化学家贝采利乌斯提出有机化学的概念,使之成为化学的一个重要分支
D.德国化学家维勒用氰酸铵合成尿素,从而打破了无机物和有机物的界限
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com