
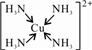
 ,在配合物Fe(SCN)2+中,提供空轨道接受孤对电子的微粒是Fe3+,故答案为:产生蓝色沉淀;Cu2++2 NH3?H2O=Cu(OH)2↓+2NH4+;难溶物溶解得到深蓝色的透明溶液;Cu(OH)2+4 NH3=[Cu(NH3)4]2++2OH-;
,在配合物Fe(SCN)2+中,提供空轨道接受孤对电子的微粒是Fe3+,故答案为:产生蓝色沉淀;Cu2++2 NH3?H2O=Cu(OH)2↓+2NH4+;难溶物溶解得到深蓝色的透明溶液;Cu(OH)2+4 NH3=[Cu(NH3)4]2++2OH-; ;Fe3+;
;Fe3+;

科目:高中化学 来源: 题型:
| A、1 mol H2O的质量为18g/mol |
| B、CH4的摩尔质量为16g |
| C、6.02×1023个SO2分子的质量为64g |
| D、标准状况下,1 mol任何物质体积均为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,写出制取过程的化学方程式.
,写出制取过程的化学方程式.查看答案和解析>>
科目:高中化学 来源: 题型:
 右图是冰醋酸(醋酸晶体)加水溶解并不断稀释过程中溶液导电能力与加入水的体积的变化关系,试回答:
右图是冰醋酸(醋酸晶体)加水溶解并不断稀释过程中溶液导电能力与加入水的体积的变化关系,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH+HCl=NaCl+H2O | ||||
B、2NaHCO3
| ||||
| C、Fe+CuSO4=Cu+FeSO4 | ||||
| D、NH3+HCl=NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式
请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | (1) | (2) | ||||||
| 3 | (3) | (4) | (5) | (6) | (7) | (8) | (9) | |
| 4 | (10) | (11) | (12) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com