
��13�֣���.ijѧУ�о���ѧϰС�鿪չ����ͬ�����Ի�ѧ��Ӧ����Ӱ���̽�������⣬ѡ��4 mL 0.01 mol��L-1KMnO4��Һ��2 mL 0.1 mol��L-1 H2C2O4��Һ����ʵ�飬�ı��������£�
|
��� |
10%����������mL�� |
�¶�/�� |
�������� |
|
�� |
2 mL |
20 |
|
|
�� |
2 mL |
20 |
10�α���MnSO4��Һ |
|
�� |
2 mL |
30 |
|
|
�� |
1 mL |
20 |
1 mL����ˮ |
��1������о������Ի�ѧ��Ӧ���ʵ�Ӱ�죬ʹ��ʵ�� �� ���â�~�ܱ�ʾ����ͬ��������о��¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬ʹ��ʵ�� �� ��
��2���Ա�ʵ��ٺ͢ܣ������о� �Ի�ѧ��Ӧ���ʵ�Ӱ�죬ʵ����м���1 mL����ˮ��Ŀ���� ��
��.��С��������ϵ�֪��C2O42-��MnO4����H���� CO2����Mn2����H2O��δ��ƽ��,�����ø÷�Ӧ�ⶨij�����ƣ�Na2C2O4����Ʒ�в����Ƶ�������������С�����1.34 g��������Ʒ����ϡ�����У�Ȼ����0.200 mol��L-1�����Ը��������Һ���еζ������е����ʲ���������غ�ϡ���ᷴӦ����
��1���ζ�ǰ�Ƿ�Ҫ�μ�ָʾ���� ����ǡ�������˵������ ��
��2���ζ�ʱ�� ����a��b���ζ���ʢװKMnO4����Һ��

��3���ﵽ�յ�ʱ������15.00 mL�ĸ��������Һ����Ʒ�в����Ƶ���������Ϊ ��
��.��1���ٺ͢� ��1�֣� �� �� �� �� ��1�֣�
��2�������Ũ�Ȼ�������Ũ�ȣ�2�֣��� ȷ���ٺ͢���Ա�ʵ����c(KMnO4)��c(H2C2O4)Ũ�Ȳ����ȷ����Һ��������� ��2�֣�
��1���� ��KMnO4��Һ����ɫ����ζ��յ���ɫ������ȥ����2�֣�
��2��b ��2�֣� ��3��75% ��3�֣�
����������.��1��Ҫ�о������Ի�ѧ��Ӧ���ʵ�Ӱ�죬����������Ӧ������ͬ�ģ�����Ӧ����ʵ��ٺ͢ڡ�ͬ��Ҫ�о��¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬��������ҲӦ������ͬ�ģ�����Ӧ����ʵ��ٺۡ͢�
��2���Ա�ʵ��ٺܿ͢�֪�����Ũ���Dz�ͬ�ģ����Կ����о������Ũ�Ȼ�������Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�졣����ʵ���������������2ml������Ϊȷ���ٺ͢���Ա�ʵ����c(KMnO4)��c(H2C2O4)Ũ�Ȳ����ȷ����Һ��������䣬��Ҫ����1mlˮ��
��1����������KMnO4��Һ����ɫ����ζ��յ���ɫ������ȥ�����Բ���Ҫ����ָʾ����
��2�����Ը��������Һ����ǿ�����ԣ��ܸ�ʴ������Ӧ������ʽ�ζ��ܡ�
��3��15.00 mL������ص����ʵ�����0.2000mol/L��0.015L��0.003mol���õ�������0.003mol��5��0.015mol�����Ը��ݵ��ӵ�ʧ�غ��֪�������Ƶ����ʵ�����0.015mol��2��0.0075mol��������0.0075mol��134g/mol��1.005g�������������Ϊ1.005g��1.34g��100����75����


 ���ѵ����Ԫ��ĩ���100��ϵ�д�
���ѵ����Ԫ��ĩ���100��ϵ�д� ��˼άС�ھ�100����ҵ��ϵ�д�
��˼άС�ھ�100����ҵ��ϵ�д� ��ʦָ��һ��ͨϵ�д�
��ʦָ��һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
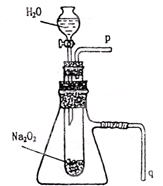 ����֬����סԼ0.2g�������Ʒ�ĩ������ʯ�����ϣ�����֬���ϵ�ˮ���ɹ۲쵽��֬����ȼ��������
����֬����סԼ0.2g�������Ʒ�ĩ������ʯ�����ϣ�����֬���ϵ�ˮ���ɹ۲쵽��֬����ȼ���������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
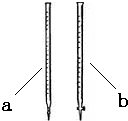 ��ijѧУ�о���ѧϰС�鿪չ����ͬ�����Ի�ѧ��Ӧ����Ӱ���̽�������⣬ѡ��4mL 0.01mol?L-1KMnO4��Һ��2mL 0.1mol?L-1 H2C2O4��Һ����ʵ�飬�ı��������£�
��ijѧУ�о���ѧϰС�鿪չ����ͬ�����Ի�ѧ��Ӧ����Ӱ���̽�������⣬ѡ��4mL 0.01mol?L-1KMnO4��Һ��2mL 0.1mol?L-1 H2C2O4��Һ����ʵ�飬�ı��������£�| ��� | 10%����������mL�� | �¶�/�� | �������� |
| �� | 2mL | 20 | |
| �� | 2mL | 20 | 10�α���MnSO4��Һ |
| �� | 2mL | 30 | |
| �� | 1mL | 20 | 1mL����ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
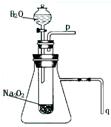 ����ʾʵ�飺����֬����סԼ0.2g�������Ʒ�ĩ������ʯ�����ϣ�����֬���ϵ�ˮ���ɹ۲쵽��֬����ȼ��������
����ʾʵ�飺����֬����סԼ0.2g�������Ʒ�ĩ������ʯ�����ϣ�����֬���ϵ�ˮ���ɹ۲쵽��֬����ȼ���������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ѡ�� | ���缫 | ����� | ������Ӧ | ������Ӧ |
| A | ���� | NaOH | 2Al-6e-+8OH-=2AlO2-+4H2O | 6H2O+6e-=6OH-+3H2�� |
| B | ���� | ϡ���� | 2Al-6e-=2Al3+ | 6H++6e-=3H2�� |
| C | ���� | Ũ���� | Mg+2e-=Mg2+ | 2NO3-+4H+-4e-=2NO2��+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
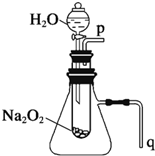 ����֬����סԼ0.2g�������Ʒ�ĩ������ʯ�����ϣ�����֬���ϵ�ˮ���ɹ۲쵽��֬����ȼ��������
����֬����סԼ0.2g�������Ʒ�ĩ������ʯ�����ϣ�����֬���ϵ�ˮ���ɹ۲쵽��֬����ȼ���������鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com