
 ��1���ü���������һ�����۵����ⷽ�����йص��Ȼ�ѧ����ʽ���£�
��1���ü���������һ�����۵����ⷽ�����йص��Ȼ�ѧ����ʽ���£����� ��1����A���ɷ�Ӧ��-�ٿɼ���H2O��g��=H2��g��+$\frac{1}{2}$O2��g���ġ�H����̬ˮ��������Һ̬ˮ�����ߣ�
B������֮�ȵ��ڻ�ѧ����ʽ������֮�ȣ�������������Ӧ����֮�ȣ�
C����Ӧ��Ϊ�����������ķ�Ӧ������ѹǿ��ƽ�������ƶ���
D��ά�ֺ㶨�¶ȣ�������ų���������ȣ�
��CH4��g��+H2O��g��?CO��g��+3H2��g��
��ʼ 1 3 0 0
ת�� 0.5 0.5 0.5 1.5
ƽ�� 0.5 2.5 0.5 1.5
KΪ������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ�
��2���ɢ٢ڼ�����������������֪��Na2FeO2��Na2Fe2O4������Ӧ��
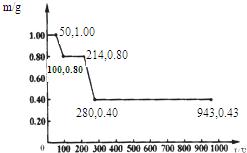
��3����ͼ���е����ݿ�֪�����ȵ�50�治������Ӧ�����ȵ�100�桫214��ʱ����ʧȥ�ᾧˮ�ķ�Ӧ�������ڼ��٣�214�桫280�淢���ֽⷴӦ�����ݷ����ķ�Ӧ���㣬�Դ���������
��� �⣺��1����A���ɷ�Ӧ��-�ٿɼ���H2O��g��=H2��g��+$\frac{1}{2}$O2��g���ġ�H=+252kJ•mol-1����2H2O��g��=2H2��g��+O2��g����H=+504kJ•mol-1����̬ˮ��������Һ̬ˮ�����ߣ���A����
B������Ӧ���Цԣ�CH4����=�ԣ�CO����ʱ������֮�ȵ��ڻ�ѧ����ʽ������֮�ȣ�Ϊ����Ӧ����֮�ȣ����ܱ����÷�Ӧ��ƽ��״̬����B����
C����Ӧ��Ϊ�����������ķ�Ӧ������ѹǿ��ƽ�������ƶ������Է�Ӧ�٢��м����ת���ʾ���С����C��ȷ��
D��ά�ֺ㶨�¶ȣ�������ų���������ȣ���Ӧ����ͬʱ������Ӧ�����ʱ�����ļ�������ʵ���֮��Ϊ$\frac{216}{36}$=6��1����D��ȷ��
�ʴ�Ϊ��CD��
��CH4��g��+H2O��g��?CO��g��+3H2��g��
��ʼ 1 3 0 0
ת�� 0.5 0.5 0.5 1.5
ƽ�� 0.5 2.5 0.5 1.5
K=$\frac{0.5��1��{5}^{3}}{0.5��2.5}$=1.35��
�ʴ�Ϊ��1.35��
��2���ɢ٢ڼ�����������������֪��Na2FeO2��Na2Fe2O4������Ӧ���÷�ӦΪNa2FeO2+Na2Fe2O4+2H2O=Fe3O4��+4NaOH��
�ʴ�Ϊ��Na2FeO2+Na2Fe2O4+2H2O=Fe3O4��+4NaOH��
��3�����辧��ȫ��ʧȥ�ᾧˮ���ɲ���������Ϊx��
MnC2O4•2H2O$\frac{\underline{\;\;��\;\;}}{\;}$MnC2O4+2H2O
179 143
1.000g x
���x��0.8g��
����ͼ����ֵ������֪��214��ʱ���ᾧˮ��ȫ��ʧȥ��ʣ�����ijɷ�ΪMnC2O4��
280��ʱ���ɹ��������ڼ�С��������̷ֽ����ɵ��������̺�һ����̼��������̼��
����������������Ϊy��
MnC2O4$\frac{\underline{\;\;��\;\;}}{\;}$MnO+CO2��+CO��
143 71
0.8g y
���y��0.4g��
��280��ʱ�ֽ���ȫ��ʣ�����ijɷ�ΪMnO��
�ʴ�Ϊ��MnC2O4��MnO��
���� ���⿼���˷�Ӧ�ȵļ��㡢ƽ��״̬���жϡ�K���йؼ��㡢���ݷ���ʽ�ļ���ȣ������ڿ���ѧ���Ի���֪ʶ���ۺ�Ӧ�������ͼ�����������Ŀ�Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ӻ������п��ܺ��й��ۼ� | |
| B�� | �ڹ��ۻ�������һ�����й��ۼ� | |
| C�� | �����Ӽ��Ļ�����һ�������ӻ����� | |
| D�� | ���й��ۼ��Ļ�����һ���ǹ��ۻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ�ų�251.2 kJ������ | B�� | �÷�Ӧ����251.2 kJ������ | ||
| C�� | �÷�Ӧ�ų�125.6 kJ������ | D�� | �÷�Ӧ����125.6 kJ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | BҲ����O2������ֱ��ת��ΪD | |
| B�� | ��X��ǿ��ʱ��A������Na2S��F��H2SO4 | |
| C�� | ��X��ǿ��ʱ��������B��Cl2�����ķ�ӦΪ��3Cl2+2NH3�TN2+6HCl | |
| D�� | ����X��ǿ�ỹ��ǿ���һ�������£�B��D�������Ӧ����C���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3������N2��=������H2�� | B�� | ������N2��=������NH3�� | C�� | ������N2��=3������H2�� | D�� | 2������H2��=3������NH3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | X��Y��Z | B�� | Y��X��Z | C�� | X��Z��Y | D�� | Y��Z��X |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
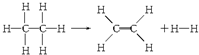
| ��ѧ�� | C-H | C=C | C-C | H-H |
| ���ܣ�kJ/mol�� | 414.4 | 615.3 | 347.4 | 435.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 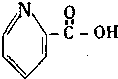 ά���� | B�� | 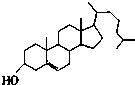 ���̴� | ||
| C�� | 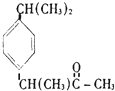 �ұص� | D�� | 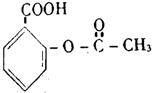 ��˹ƥ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com