
在下列变化中,需要加入合适的氧化剂才能实现的是( )
|
| A. | HCl→H2 | B. | CO2→CO | C. | Fe2O3→Fe | D. | Br﹣→Br2 |
考点:
氧化还原反应.
专题:
氧化还原反应专题.
分析:
需要加入合适的氧化剂才能实现,则选项中为还原剂的变化,还原剂中某元素的化合价升高,以此来解答.
解答:
解:A.HCl→H2中,H元素的化合价降低,一般需要加还原剂才能实现,故A不选;
B.CO2→CO中,C元素的化合价降低,一般需要加还原剂才能实现,故B不选;
C.Fe2O3→Fe中,Fe元素的化合价降低,一般需要加还原剂才能实现,故C不选;
D.Br﹣→Br2中,Br元素的化合价升高,则需要加氧化剂实现,故D选;
故选:D.
点评:
本题考查氧化还原反应,为高考常见题型,侧重还原剂和氧化剂的反应的考查,注意把握反应中元素的化合价变化为解答的关键,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,CH4产量随光照时间的变化如下图所示。
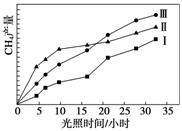
(1)在0~30小时内,CH4的平均生成速率vⅠ、vⅡ、vⅢ从大到小的顺序为________________;反应开始后的12小时内,在第______种催化剂作用下,收集的CH4最多。
(2)将所得CH4与H2O(g)通入聚焦太阳能反应器,发生反应:CH4(g)+H2O(g)CO(g)+3H2(g)。该反应ΔH=206 kJ·mol-1。
①在下列坐标图中,画出反应过程中体系能量变化图(进行必要标注)。
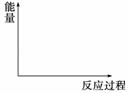
②将等物质的量的CH4和H2O(g)充入1 L恒容密闭反应器,某温度下反应达平衡,平衡常数K=27,此时测得CO的物质的量为0.10 mol,则CH4的平衡转化率为________(计算结果保留两位有效数字)。
(3)已知:CH4(g)+2O2(g)===CO2(g)+2H2O(g)
ΔH=-802 kJ·mol-1
写出由CO2生成CO的热化学方程式:______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、M、W为五种短周期元素.X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g•L﹣1;W的质子数是X、Y、Z、M四种元素质子数之和的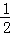 .下列说法正确的是( )
.下列说法正确的是( )
A. 原子半径:W>Z>Y>X>M
B. XZ2、X2M2、W2Z2均为直线型的共价化合物
C. 由X元素形成的单质不一定是原子晶体
D. 由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | 同温同压下,相同体积的物质,它们的物质的量必相等 |
|
| B. | 任何条件下,等物质的量的乙烯和一氧化碳所含的分子数必相等 |
|
| C. | 1L一氧化碳气体一定比1L氧气的质量小 |
|
| D. | 等体积、等物质的量浓度的强酸中所含的H+数一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
|
| A. | 将硫酸钡放入水中不能导电,所以硫酸钡不是电解质 |
|
| B. | CO2溶于水得到的溶液能导电,所以CO2是电解质 |
|
| C. | 金属能导电,所以金属是电解质 |
|
| D. | 固态的氯化钠不导电,熔融态的氯化钠可以导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于原子结构、元素性质的说法正确的是( )
|
| A. | 非金属元素组成的化合物中只含共价键 |
|
| B. | ⅠA族金属元素是同周期中金属性最强的元素 |
|
| C. | 同种元素的原子均有相同的质子数和中子数 |
|
| D. | ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com