
分析 (1)根据准确配制一定体积一定物质的量浓的溶液用到的仪器来回答;
(2)残缺方程式配平首先确定缺什么,根据电子转移守恒,配平化学方程式;
(3)酸式滴定管可以量取具有强氧化性的溶液,高锰酸钾具有颜色,锰离子无色;
(4)根据化学方程式计算消耗过氧化氢的量然后计算质量分数;
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则消耗的标准溶液的体积偏大.
解答 解:(1)准确配制一定体积一定物质的量浓的溶液用容量瓶;
故答案为:容量瓶;
(2)方程式中,高锰酸钾有强氧化性,能将双氧水氧化为氧气,先确定缺的是O2,锰元素化合价降低了5价,生成1mol氧气时,氧元素化合价升高2价,根据电子转移守恒,配平化学方程式高锰酸根前面的系数为2,双氧水前面的系数为5,根据原子守恒来配平其他物质前面的系数,离子方程式2MnO4-+5H2O2+6H+=2Mn2++8H2O+502↑,
故答案为:2、5、6、2、8、5O2;
(3)由于高锰酸钾标准溶液具有强氧化性,所以只能使用酸式滴定管,滴定到达终点的现象是:滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色,
故答案为:酸式;滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色;
(4)根据化学方程式可以得到关系式:2MnO4-~5H2O2,耗用c mol/L KMnO4标准溶液V mL,即cV×10-3mol的高锰酸钾时,所用双氧水的物质的量:2.5cV×10-3mol,则原过氧化氢的质量为:0.025cVmol×34g/mol=0.85cV,过氧化氢溶液中过氧化氢的质量分数为:$\frac{0.85cV}{10.00mL×ρg/mL}$=$\frac{0.085cV}{ρ}$,
故答案为:$\frac{0.085cV}{ρ}$;
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则消耗的标准溶液的体积偏大,所以计算的KMnO4的物质的量偏大,则过氧化氢的物质的量偏大,所以测得结果偏高;
故答案为:偏高.
点评 本题是一道综合知识题目,涉及仪器的选择、离子方程式的配平、滴定终点的确定、质量分数的计算,要求学生具有分析和解决问题的能力,注意把握中和滴定实验原理和操作方法,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | △H>0、△S<0 | B. | △H>0、△S>0 | C. | △H<0、△S<0 | D. | △H<0、△S>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
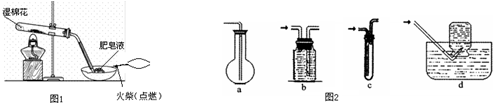
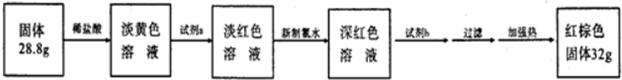
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测液体积/mL | 标准盐酸体积/mL | |
| 滴定前读数 | 滴定后读数 | ||
| 第1次 | 20.00 | 4.10 | 29.10 |
| 第2次 | 20.00 | 0.00 | 24.90 |
| 第3次 | 20.00 | 4.00 | 29.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
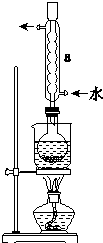 Na2S2O3是重要的化工原料,易溶于水.在中性或碱性环境中稳定.
Na2S2O3是重要的化工原料,易溶于水.在中性或碱性环境中稳定.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定 次数 | 待测溶液的体积(mL) | 0.100 0mol•L-1NaOH的体积(mL) | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积(mL) | ||
| 第一次 | 20.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 20.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 20.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
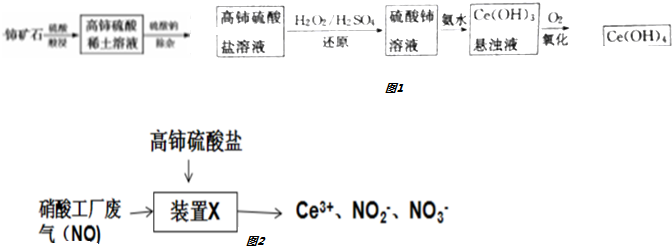
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com