
| A、能与金属钠反应放出氢气 |
| B、能发生加聚反应生成高分子化合物 |
| C、能与新制氢氧化铜反应 |
| D、能与溴水发生氧化反应使其褪色 |
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
| 实验 编号 | T/K | 催化剂的用量/g | 酸性KMnO4溶液的浓度/mol?L-1 | 实验目的 |
| ① | 298 | 0.5 | 0.010 | a.实验①和②探究酸性KMnO4溶液的浓度对该反应速率的影响; b.实验①和 c.实验①和 |
| ② | ||||
| ③ | ||||
| ④ |
| 实验编号 | 溶液褪色所需时间 t/min | ||
| 第1次 | 第2次 | 第3次 | |
| ① | 14.0 | 13.0 | 11.0 |
| ② | 6.0 | 7.0 | 7.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
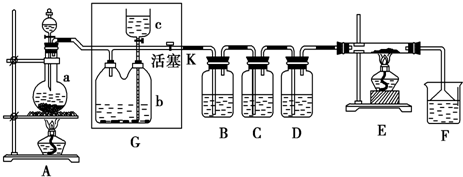
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合气体中一定有甲烷 |
| B、混合气体一定是甲烷和乙烯 |
| C、混合气体中一定没有乙炔 |
| D、混合气体中一定有丙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:
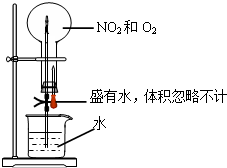 用如图所示的装置做喷泉实验,该实验条件下的气体摩尔体积为a L/mol,且不考虑2NO2?N2O4.最终液体充满了烧瓶,则烧瓶内溶液的物质的量浓度约是( )
用如图所示的装置做喷泉实验,该实验条件下的气体摩尔体积为a L/mol,且不考虑2NO2?N2O4.最终液体充满了烧瓶,则烧瓶内溶液的物质的量浓度约是( )A、
| ||
B、
| ||
C、
| ||
| D、无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、难溶电解质的溶度积越小,溶解度越大 |
| B、可以通过沉淀反应使杂质离子完全沉淀 |
| C、难溶电解质的溶解达到平衡后就静止不动了 |
| D、一定浓度的NH4Cl溶液可以溶解Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、A的转化率增大 |
| B、平衡向逆反应方向移动 |
| C、平衡没有移动 |
| D、上述三种情况都有可能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com