
【题目】对于1L H2SO4和HNO3的混合溶液,若H2SO4和HNO3物质的量浓度存在如下关系:c(H2SO4)+c(HNO3)=1.2mol/L,则理论上最多能溶解铜的物质的量为
A. 0.40mol B. 0.45mol C. 0.72mol D. 0.80mol
【答案】C
【解析】
铜与稀硫酸不反应,但和稀硝酸反应。离子方程式3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,硫酸电离出的氢离子可参与反应,由此进行计算。
铜不与硫酸反应,但能提供氢离子。硝酸与铜反应,生成硝酸铜,硝酸根离子与硫酸提供的氢离子可以继续反应,离子方程式为3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,硝酸根离子的浓度与氢离子的浓度比为1:4时,溶解的铜最多。
设硫酸的物质的量为x mol,硝酸的物质的量为y mol,则x+y=1.2,y:(2x+y)=1:4,解得x=0.72mol,y=0.48mol。故参加反应的铜的最大量n(Cu)=n(NO3-)×![]() =0.48mol×
=0.48mol×![]() =0.72mol。
=0.72mol。
本题选C。


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:
【题目】根据以下两幅图,可判断出下列离子方程式中错误的是( )

A. 2Ag(s)+Cd2+(aq)=2Ag+(aq)+Cd(s)
B. Co2+(aq)+Cd(s)=Co(s)+Cd2+(aq)
C. 2Ag+(aq)+Cd(s)=2Ag(s)+Cd2+(aq)
D. 2Ag+(aq)+Co(s)=2Ag(s)+Co2+(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自来水常用氯气消毒,某学生用这种自来水去配制下列物质溶液,不会产生明显的药品变质问题的是 ( )
A. AgNO3 B. FeCl2
C. NaHSO3 D. NaNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe、CO、Ni均为第Ⅷ族元素,它们的化合物在生产生活中有着广泛的应用。
(1)基态CO原子的价电子排布式为____________,Co3+核外3d能级上有_________对成对电子。
(2)Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co+ 的配位数是______________,1mol 配离子中所含σ键的数目为_____________,配位体N3-中心原子杂化类型为____________________。
(3)Co2+在水溶液中以[Co(H2O)6]2+存在。向含Co2+的溶液中加入过量氨水可生成更稳定的[Co(NH3)6]2+ ,其原因是___________________。
(4)某蓝色晶体中,Fe2+、Fe3+分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个CN-,K+位于立方体的某恰当位置上。据此可知该晶体的化学式为____________,立方体中Fe2+间连接起来形成的空间构型是_____________________。
(5)NiO的晶体结构如图甲所示,其中离子坐标参数A 为(0,0,0),B为(1,1,0),则C离子坐标参数为_______________。

(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图乙),已知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为__________g(用含a、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国研究锂硫电池获得突破,电池的总反应是16Li+S8 ![]() 8Li2S ,充放电曲线如图所示,下列说法不正确的是( )
8Li2S ,充放电曲线如图所示,下列说法不正确的是( )
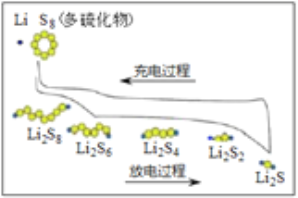
A. 充电时,电能转化为化学能
B. 放电时,锂离子向正极移动
C. 放电时,1mol Li2S6转化为Li2S4得到2mole-
D. 充电时,阳极总电极反应式是8S2- -16e- = S8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置,甲中盛有100mL 0.1mol/LCuSO4溶液,乙中盛有100mL 0.2mol/L Na2SO4溶液。
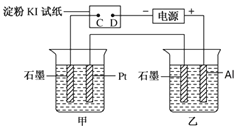
(1)通电一段时间,观察到湿润的淀粉KI试纸的_____(选填“C” 或“D”)端变蓝。
(2)装置乙中Al极的电极反应式为:_____________________。一段时间后观察到装置乙中的现象是:_________________。
(3)若电解一段时间后,装置甲中收集到气体0.056 L(标准状况下),则:装置甲中发生反应的离子反应方程式为______________________________。
(4)若电解一段时间后,装置甲中溶液需加入0.005molCu2(OH)2CO3才能恢复原来的浓度和pH,则电解过程中转移电子的物质的量为__________。
(5)某新型燃料电池,以甲醇为燃料,另一极通入一定量的CO2和O2的混合气体。一定比例的Li2CO3和Na2CO3的熔融混合物为电解质,则负极反应式为______________。正极反应式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸钴[Co(H2PO2)2·6H2O]可用于化学电镀,共饱和溶液的pH约为6;利用电渗析法可在产品室析出高纯[Co(H2PO2)2·6H2O]电渗析原理如图所示。则阳离子交换膜有
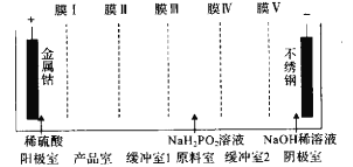
A. 1个 B. 2个 C. 3个 D. 4个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大:W、X、Y、Z组成的单质可发生如图所示的化学反应;B是生活中最常见的液体;常温下Y、Z组成的二元化合物的水溶液pH=7。下列说法错误的是
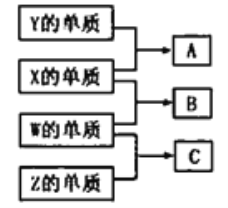
A. A与B的反应一定是化合反应
B. 离子半径:Z>X>Y>W
C. W、Y、Z均存在两种或两种以上的氧化物
D. 将等物质的量的A、C溶于同一烧杯水中,所得溶液的pH一定大于7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用双线桥及单线桥表示反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O 电子转移情况。
双线桥________________________________________。
单线桥________________________________________。
该反应中氧化剂是:_______。若有4molHNO3参加反应,转移电子的物质的量为______mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com