
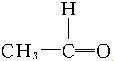 +
+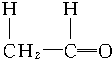 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$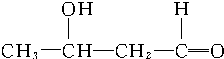
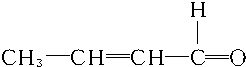 +2H2$→_{△}^{催化剂}$
+2H2$→_{△}^{催化剂}$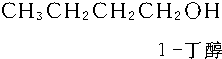
分析 据已知反应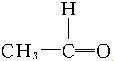 +
+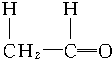 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$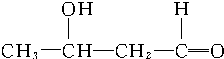 ,以乙烯为原料合成1-丁醇的步骤可以是:①乙烯氧化为乙醛,②羟醛缩合生成2-羟基丁醛,③2-羟基丁醛发生消去反应生成CH3CH=CHCHO,④CH3CH=CHCHO与足量氢气发生加成反应生成1-丁醇,据此分析.
,以乙烯为原料合成1-丁醇的步骤可以是:①乙烯氧化为乙醛,②羟醛缩合生成2-羟基丁醛,③2-羟基丁醛发生消去反应生成CH3CH=CHCHO,④CH3CH=CHCHO与足量氢气发生加成反应生成1-丁醇,据此分析.
解答 解:以乙烯为原料合成1-丁醇的步骤可以是:①乙烯氧化为乙醛,②羟醛缩合生成2-羟基丁醛,③2-羟基丁醛发生消去反应生成CH3CH=CHCHO,④CH3CH=CHCHO与足量氢气发生加成反应生成1-丁醇,反应方程式为:①2CH2═CH2+O2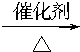 2CH3-CHO
2CH3-CHO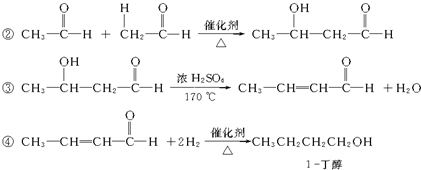 ,
,
故答案为:①2CH2═CH2+O2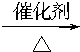 2CH3-CHO
2CH3-CHO .
.
点评 本题考查有机物的合成,注意结合物质结构及反应信息进行推断,难度中等,注意掌握官能团的性质与相互转化,结合反应信息设计合成路线.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
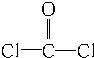 和双酚A:
和双酚A: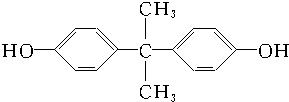 缩聚而成,其反应方程式为
缩聚而成,其反应方程式为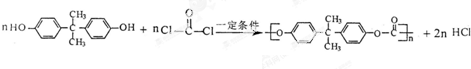 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲醛是甲基跟醛基相连而构成的 | |
| B. | 饱和一元醛的通式可简写为RCOH | |
| C. | 在银镜反应中乙醛体现了氧化性 | |
| D. | 饱和一元脂肪醛的分子组成符合通式CnH2nO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C6H12N4 | B. | C4H8N4 | C. | C6H10N4 | D. | C6H8N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 $\stackrel{R′OH}{→}$
$\stackrel{R′OH}{→}$ +
+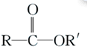
 +RCl→
+RCl→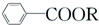 +NaCl
+NaCl .
. +
+ $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O.
+H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
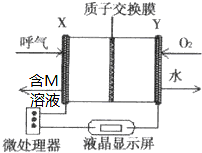 查处酒后驾驶所采用的“便携式乙醇测量仪”,以燃料电池为工作原理,如图,两电极材料均为Pt.理论上乙醇可以被完全氧化为CO2,但实际乙醇被氧化为M,其中一个电极的反应式为:CH3CH2OH-2e-→M+2H+.下列说法中正确的是( )
查处酒后驾驶所采用的“便携式乙醇测量仪”,以燃料电池为工作原理,如图,两电极材料均为Pt.理论上乙醇可以被完全氧化为CO2,但实际乙醇被氧化为M,其中一个电极的反应式为:CH3CH2OH-2e-→M+2H+.下列说法中正确的是( )| A. | 电池内部H+向X极移动 | |
| B. | 另一极Y极的电极反应式为:O2+4e-+2H2O=4OH- | |
| C. | 乙醇在X极上发生还原反应,电子经过外电路流向Y极 | |
| D. | 电池总反应为:2CH3CH2OH+O2→2CH3CHO+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com