
(12分)一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以Co2O3·CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中。从废料中回收氧化钴(CoO)的工艺流程如下:

(1)过程I中采用NaOH溶液溶出废料中的Al,反应的离子方程式为 。
(2)过程II中加入稀H2SO4酸化后,再加入Na2S2O3溶液,加入Na2S2O3的作用是___________。在实验室模拟工业生产时,也可用盐酸代替酸化的Na2S2O3,但实际工业生产中不用盐酸,请从反应原理分析不用盐酸浸出钴的主要原因_________。
(3)用离子方程式表示过程Ⅳ中Na2CO3的主要作用_______。
(4)下图是CoCl2·6H2O晶体受热分解时,剩余固体质量随温度变化的曲线,B物质的化学式是______。

(1)2Al+2OH-+2H2O = 2AlO- 2+3H2↑(2)还原Co3+ (其它合理答案也给分)Co2O3·CoO可氧化盐酸产生Cl2,污染环境。(其它合理答案也给分)(3)CO32-+Co2+= CoCO3↓(4)CoCl2?H2O
【解析】
试题分析:(1)铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,离子反应方程式为:
2Al+2OH-+2H2O=2AlO2-+3H2↑;(2)根据题意知,Co2O3·CoO和Na2S2O3在酸性条件下发生氧化还原反应生成CoSO4、Na2SO4和H2O,加入Na2S2O3的作用是还原Co3+ ;盐酸具有还原性,能被Co2O3?CoO氧化生成有毒的氯气而污染环境;(3)碳酸钠溶液在过程Ⅳ中调整pH,提供CO32-,使Co2+沉淀为CoCO3;离子方程式为CO32-+Co2+= CoCO3↓;(4)根据题给图像知,
CoCl2?6H2O~CoCl2
238 130
m 65mg
解得:m=119mg
设 A物质的化学式为CoCl2?nH2O,则有:
CoCl2?6H2O~CoCl2?nH2O △m
238 18(6-n)
119mg 119mg-83mg
解得:n=2,所以A物质的化学式为:CoCl2?2H2O。
考点:考查铝等金属及其化合物的性质、氧化还原反应、离子反应、关系式法计算等。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源:2013-2014重庆市主城七区高三下学期第二次联考理综化学试卷(解析版) 题型:简答题
(14分)硫代硫酸钠(Na2S2O3)俗称保险粉,可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等。实验室可通过如下反应制取:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2。
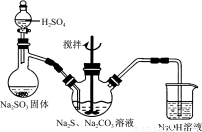
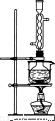
图1 图2
(1)用图1所示装置制取Na2S2O3,其中NaOH溶液的作用是_____________________。
如将分液漏斗中的H2SO4改成浓盐酸,则三颈烧瓶内除Na2S2O3生成外,还有
(填化学式)杂质生成。
(2)为测定所得保险粉样品中Na2S2O3·5H2O的质量分数,可用标准碘溶液进行滴定,
该反应的化学方程式为:2Na2S2O3+I2 = 2NaI+Na2S4O6
①利用KIO3、KI和HCl作原料可配制标准碘溶液。写出配制时所发生反应的离子方程式 。
②准确称取一定质量的Na2S2O3·5H2O样品于锥形瓶中,加水溶解,并滴加______作指示剂,用所配制的标准碘溶液滴定。滴定时所用的玻璃仪器除锥形瓶外,还有 。
③若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O3·5H2O的质量分数的测量结果___________(填“偏高”“偏低”或“不变”)。
(3)本实验对Na2S的纯度要求较高,利用图2所示的装置可将工业级的Na2S提纯。已知Na2S常温下微溶于酒精,加热时溶解度迅速增大,杂质不溶于酒精。
提纯步骤依次为:
①将已称量好的工业级Na2S放入圆底烧瓶中,并加入一定质量的酒精和少量水;
②按图2所示装配所需仪器,向冷凝管中通入冷却水,水浴加热;
③待 时,停止加热,将烧瓶取下;
④ __________________________;
⑤ __________________________;
⑥将所得固体洗涤、干燥,即可得到Na2S·9H2O晶体。
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆一中高二下学期期末考试化学试卷(解析版) 题型:选择题
下列物质分类正确的是
A.苯和溴苯均为芳香烃 B.酚醛树脂和聚乙烯均为体型高分子材料
C.葡萄糖和麦芽糖均为还原性糖 D.油脂和淀粉均为天然高分子化合物
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆一中高一下学期期末考试化学试卷(解析版) 题型:选择题
下列排列顺序正确的是
A.熔点:MgBr2> Cs > Na
B.微粒半径:Ca2+ > C1- > Mg2+
C.碱性:KOH > Mg(OH)2 > Al(OH)3
D.氧化性:Cu2+ > Fe3+ > K+
查看答案和解析>>
科目:高中化学 来源:2013-2014辽宁省大连市高三双基测试化学试卷(解析版) 题型:推断题
【选修5-有机化学基础】(15分)
已知:稀碱液中卤苯难水解。芳香族化合物C的分子式为C9H9OCl。C分子中有二条侧链,苯环上一氯代物只有二种,其核磁共振氢谱图中有五个吸收峰,吸收峰的面积之比为1∶2∶2∶2∶2。在一定条件下,由物质C可发生如图所示的转化:
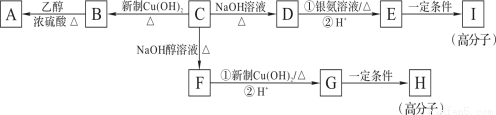
(1)C→F的反应类型是_______;H的结构简式是________;
(2)C分子中的官能团名称 ,最少有_____个碳原子共面;
(3)写出下列化学方程式:D与银氨溶液反应_________;E→I________;
(4)D的一种同系物W分子式为C8H8O2。则符合下列条件的W的同分异构体的结构简式 。
条件:①属于芳香族化合物 ②遇FeCl3溶液不变紫色 ③1 mol W可与含2 mol NaOH的溶液反应
查看答案和解析>>
科目:高中化学 来源:2013-2014辽宁省大连市高三双基测试化学试卷(解析版) 题型:选择题
下列实验步骤与实验事实的相应结论解释正确的是
选项 | 实验步骤与实验事实 | 结论解释 |
A | Mg(OH)2、Al(OH)3混合物中加入NaOH溶液,Al(OH)3溶解而Mg(OH)2没有溶解 | Mg(OH)2Ksp比Al(OH)3的小 |
B | ZnS能溶解在稀盐酸中,CuS不能溶解在稀盐酸中 | CuS的Ksp比ZnS的小 |
C | 在溶有NH3的BaCl2溶液中通入CO2,有白色沉淀生成 | NH3在反应中作催化剂 |
D | 单质硅不溶于浓硫酸和浓硝酸 | 硅被强氧化性酸钝化 |
查看答案和解析>>
科目:高中化学 来源:2013-2014辽宁省大连市高三双基测试化学试卷(解析版) 题型:选择题
NaCl是一种化工原料,可以制备一系列物质(如图所示)。下列说法正确的是
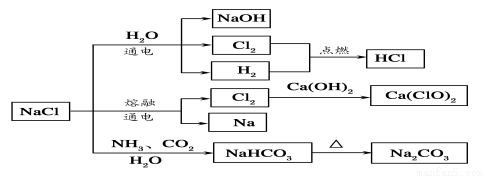
A.25℃,NaHCO3在水中的溶解度比Na2CO3的大
B.石灰乳和Cl2反应可制得漂白粉,其主要成分是次氯酸钙
C.常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应
D.如图所示转化反应不都是氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2013-2014辽宁省高三仿真测试理科综合化学试卷(解析版) 题型:选择题
分析下表中各项的排布规律,有机物X是按此规律排布的第19项,下列有关X的结构和性质说法中一定错误的是
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
CH4 | CH2O | CH2O2 | CH4O | C2H6 | C2H4O | C2H4O2 | C2H6O |
A.是戊酸,同分异构体有4种
B.是酯,在稀硫酸条件下水解的两种产物的相对分子质量不可能相等
C.可以发生银镜反应
D.可以与溴水发生加成反应
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高三高考模拟理综化学试卷(解析版) 题型:填空题
[化学——有机化学基础]
有甲、乙、丙三种物质:
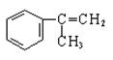
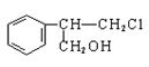

甲 乙 丙
(1) 乙中能发生消去反应的官能团为____________________。
(2)由甲转化为乙需经下列过程(已略去各步反应的部分产物,下同):
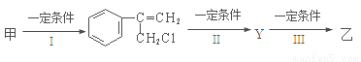
反应Ⅱ的条件是NaOH溶液、加热;反应III的化学方程式为________________________
(不需注明反应条件)。
(3)由甲出发合成丙的路线之一如下:
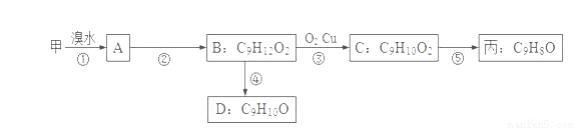
①下列物质不能与B反应的是___________(选填序号)。
a.金属钠 b.FeCl3溶液 c.Na2CO3溶液 d.HBr溶液
②C的结构简式为 __________________________;第⑤步反应类型______________________
③任写一种能同时满足下列条件的D的同分异构体的结构简式______________________。
a.苯环上的一氯代物有两种 b.遇FeCl3溶液发生显色反应 c.能与Br2/CCl4发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com