
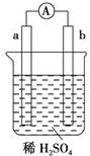
| A. | 碳棒上有气体放出,溶液pH变大 | |
| B. | a是正极,b是负极 | |
| C. | 稀硫酸中有电子流动,方向是从b极到a极 | |
| D. | a极上发生了氧化反应 |
分析 金属a能从酸中置换出H2,b为碳棒,则a属于氢之前的金属,该装置构成原电池,a为负极、b为正极,电子从负极沿导线流向正极,据此分析解答.
解答 解:金属a能从酸中置换出H2,b为碳棒,则a属于氢之前的金属,该装置构成原电池,a为负极、b为正极,
A.碳棒上氢离子得电子生成氢气,溶液中氢离子浓度减小,溶液的PH增大,故A正确;
B.通过以上分析知,a是负极、b是正极,故B错误;
C.该装置构成原电池,电子不能通过电解质溶液,故C错误;
D.a电极上金属失电子发生氧化反应,故D正确;
故选BC.
点评 本题考查了原电池原理,明确正负极的判断、电子流向、电极上的反应等知识点即可解答,注意电解质溶液中离子移动方向,为易错点.


 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “绿色化学”的理念是从源头上减少和消除工业产生对环境的污染 | |
| B. | 氢能是清洁能源,工业上电解水法制大量氢气符合节能减排理念 | |
| C. | 如将纳米材料分散到液体分散剂中,该分散系可发生丁达尔现象,由此可推测纳米材料的直径为1~100nm之间 | |
| D. | 将苦卤浓缩、氧化,鼓入热空气或水蒸气提取海水中的溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
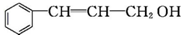 乙:
乙: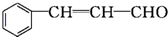
| 分子式 | C16H14O2 |
| 部分性质 | 能使Br2/CCl4褪色 |
| 能在稀硫酸中水解 |

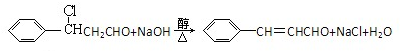 (注明反应条件).
(注明反应条件).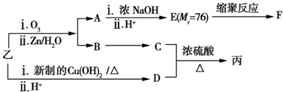
 +
+ $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$  +H2O
+H2O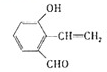 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 含有0.6mol Ca2+ | B. | 含有0.3mol Cl- | ||
| C. | n(Na+):n(OH-)=1:5 | D. | 所含元素中钙元素的质量很大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通过电解熔融CD3可以制备C单质 | |
| B. | A和B可以形成BA3、B2A4等酸性化合物 | |
| C. | C的氢氧化物可以溶于B或D的最高价氧化物的水化物 | |
| D. | BA4BO3中只存在非金属元素,只存在共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶格能 NaCl<MgO | B. | 熔点:NH3<PH3 | ||
| C. | 离子半径:Na+<O2- | D. | 第一电离能:Mg>Al |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com