
对于某些离子的检验及结论一定正确的是
A.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO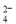
B.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+
C.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO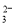
D.加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ba2+
科目:高中化学 来源:2016届河南省洛阳市高一上学期期末检测化学试卷(A)(解析版) 题型:选择题
关于硅及其化合物的叙述中,不正确的是
A.硅是良好的半导体材料
B.二氧化硅能与石灰石反应:SiO2+CaCO3 CaSiO3+CO2↑
CaSiO3+CO2↑
C.可以用焦炭还原二氧化硅生产硅:SiO2 + 2C  Si + 2CO↑
Si + 2CO↑
D.水泥的主要成分是 Na2SiO3、CaSiO3 和 SiO2
查看答案和解析>>
科目:高中化学 来源:2016届河南省平顶山市高一第一学期期末调研考试化学试卷(解析版) 题型:选择题
下列离子方程式的书写正确的是
A.铁和稀硫酸反应:2Fe + 6H+ =2Fe 3+ +3H 2↑
B.NaHCO3溶液与NaOH溶液反应: OH― + HCO3- = CO32- + H2O
C.钠和冷水反应 Na+2H2O=Na++2OH?+H2↑
D.氯化铝溶液中加入过量的氨水Al3+ +4NH3·H2O=AlO2-+4NH4++2H2O
查看答案和解析>>
科目:高中化学 来源:2016届河南省原名校高一上学期期末联考化学试卷(解析版) 题型:选择题
某澄清溶液可能含有K+、Al3+、Mg2+、NH4+、Fe2+、SO42-、CO32-中的一种或几种,为确定其成分,进行如下实验:①取部分溶液,逐滴滴入用HCl酸化的BaCl2溶液,只产生白色沉淀;②另取部分溶液,缓慢加入足量的Na2O2固体并加热,产生无色无味的气体,同时产生白色沉淀后白色沉淀部分溶解。下列推断正确的是
A.肯定有Al3+、SO42-,可能有K+、NH4+
B.肯定无NH4+、Mg2+、CO32-,可能有Fe2+
C.原溶液一定是明矾和MgSO4的混合溶液
D.肯定有Mg2+,K+只能通过焰色反应才能确定
查看答案和解析>>
科目:高中化学 来源:2016届河南省原名校高一上学期期末联考化学试卷(解析版) 题型:选择题
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是
A.2Na2O2+2H2O =4NaOH+O2↑ B.Cl2 + H2O  HClO + HCl
HClO + HCl
C.2F2+2H2O=4HF+O2 D.4Fe(OH)2+O2+2H2O=4Fe(OH)3
查看答案和解析>>
科目:高中化学 来源:2016届河北省高一下学期第一次月考化学试卷(解析版) 题型:实验题
下图甲是课本中验证铜和浓硝酸反应的装置,乙、丙是师生对演示实验改进后的装置:
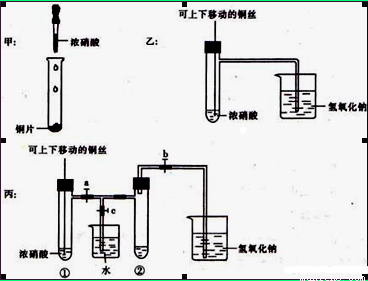
(1)甲、乙、丙三个装置中共同发生的化学方程式是 。
(2)和甲装置相比,乙装置的优点是可以控制反应的开始与停止,还可以 。
(3)为了进一步验证NO2和水的反应,当气体充满②试管后,将铜丝提起与溶液脱离。欲使烧杯中的 水进人②试管,应如何操作?
查看答案和解析>>
科目:高中化学 来源:2016届河北省高一下学期第一次月考化学试卷(解析版) 题型:选择题
现有m molNO2和n mol NO组成的混合气体,欲用a mol/L NaOH溶液使该混合气体全部转化成盐NaNO3或NaNO2进入溶液,需用该NaOH溶液的体积是
A、m/a L B.2m/3a L C.2(m+n)/3a L D.(m+n)/a L
查看答案和解析>>
科目:高中化学 来源:2016届河北省高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.同一主族相邻两个周期的元素的原子序数差一定等于上一周期所含元素种类
B.短周期元素中某元素的原子序数不可能是同主族元素原子序数的2倍
C.L层上的电子数为奇数的元素一定是主族元素
D.目前使用的长式元素周期表中,最长的周期含36种元素
查看答案和解析>>
科目:高中化学 来源:2016届江西赣州市高一上学期期末联考化学试卷(解析版) 题型:实验题
过氧化钠(Na2O2)是中学常见物质。已知:过氧化钠与CO2反应有气体生成,而将SO2通入过氧化钠粉末中也有气体生成。有人提出CO2、SO2与过氧化钠的反应原理相同,但也有人提出SO2具有较强的还原性,能被过氧化钠氧化生成硫酸钠,CO2无强还原性,反应原理不相同。据此设计如下实验操作进行判断。
实验一:向一定量的过氧化钠固体中通入足量的SO2,取反应后的固体进行实验探究,以证明过氧化物与SO2反应的特点。
(1)提出假设:假设1:反应后固体中只有________,证明SO2未被氧化;
假设2:反应后固体中只有________,证明SO2完全被氧化;
假设3:__________________________证明______________________。
实验探究:实验二:通过测量气体的体积判断发生的化学反应,实验装置如下:
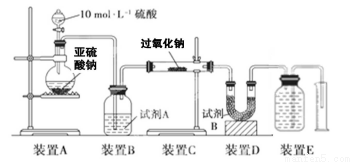
(2)试剂A可以选用________,试剂B的作用是________。
(3)实验测得装置C中过氧化钠质量增加了m1 g,装置D质量增加了m2 g,装置E中收集到的气体为V L(已换算成标准状况下),用上述有关测量数据判断, SO2未被氧化时、完全被氧化的V-m1关系式。
未被氧化:____________,完全被氧化:____________。
(4)若SO2完全被氧化,写出反应的化学方程式: __________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com