
| A. | 标准状况下,22.4L乙烯中含有的共用电子对数为6NA | |
| B. | 1L pH=13的氢氧化钡溶液中含有的OH-离子数为0.2NA | |
| C. | 46g的无水乙醇与足量乙酸在浓硫酸中加热,可生成88g乙酸乙酯 | |
| D. | 在反应KIO3+6HI═KI+3I2+3H2O中,若有1molH2O生成,则转移电子数为2NA |
分析 A、求出乙烯的物质的量,然后根据乙烯中含6对共用电子对来分析;
B、pH=13的氢氧化钡溶液中氢氧根的浓度为0.1mol/L;
C、酯化反应为可逆反应;
D、反应KIO3+6HI═KI+3I2+3H2O反应5mol电子生成3mol水.
解答 解:A、乙烯标况下22.4L的物质的量为1mol,而乙烯中含6对共用电子对,故1mol乙烯中含6NA对共用电子对,故A正确;
B、pH=13的氢氧化钡溶液中氢氧根的浓度为0.1mol/L,故1L氢氧化钡溶液中含有的氢氧根的物质的量为0.1mol,则含0.1NA个,故B错误;
C、酯化反应为可逆反应,故不能进行彻底,则生成的乙酸乙酯小于88g,故C错误;
D、反应KIO3+6HI═KI+3I2+3H2O反应5mol电子生成3mol水,故当生成1mol水时,转移的电子为$\frac{5}{3}$NA个,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 丹参素可用于祛瘀止痛、凉血消痈、养血安神.其结构简式如图.
丹参素可用于祛瘀止痛、凉血消痈、养血安神.其结构简式如图.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 ,关于该化合物的下列说法正确的是( )
,关于该化合物的下列说法正确的是( )| A. | 该有机物分子式C15H14O | |
| B. | 该有机物完全燃烧时只有二氧化碳和水两种产物 | |
| C. | 该有机物分子中含有羟基,属于醇 | |
| D. | 该有机物属于烯烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将等体积、等pH的硫酸和醋酸分别稀释相同倍数,醋酸的pH变化大 | |
| B. | 用氯化氢作导电性实验,灯光较暗,说明氯化氢是弱电解质 | |
| C. | 向滴有酚酞的氨水中逐滴加入浓硝酸,红色褪去,说明氨水中存在电离平衡 | |
| D. | 向浓度均为0.1mol•L-1的NaCl和NaI混合溶液中滴加少量AgNO3溶液,先出现黄色沉淀[已知:Ksp(AgCl)>Ksp(AgI)] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
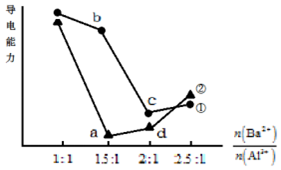 向两份20mL 0.1mol/L Ba(OH)2溶液中各加入一定量的KAl(SO4)2和Al2(SO4)3,溶液的导电性随$\frac{n(B{a}^{2+})}{n(A{l}^{3+})}$(混合前)的变化关系如右图所示.下列分析不正确的是( )
向两份20mL 0.1mol/L Ba(OH)2溶液中各加入一定量的KAl(SO4)2和Al2(SO4)3,溶液的导电性随$\frac{n(B{a}^{2+})}{n(A{l}^{3+})}$(混合前)的变化关系如右图所示.下列分析不正确的是( )| A. | ①代表加入KAl(SO4)2的变化曲线 | |
| B. | a点溶液的pH值约为7 | |
| C. | b点溶液中大量存在的阳离子有Al3+和Ba2+ | |
| D. | c、d两点溶液中Ba(OH)2均已完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
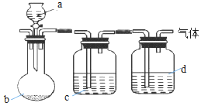 用如图装置制取、提纯并收集下表中的四种气体(a、b、c、d表示相应仪器中加入的试剂,收集装置略去).其中可行的是( )
用如图装置制取、提纯并收集下表中的四种气体(a、b、c、d表示相应仪器中加入的试剂,收集装置略去).其中可行的是( )| 气体 | a | b | c | d | |
| A | CO2 | 稀硫酸 | 石灰石 | 饱和Na2CO3溶液 | 浓H2SO4 |
| B | Cl2 | 浓盐酸 | KMnO4固体 | 饱和NaCl溶液 | 浓H2SO4 |
| C | NH3 | 饱和NH4Cl溶液 | 消石灰 | H2O | 碱石灰 |
| D | H2 | 硝酸 | 锌粒 | H2O | P2O5 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol?L-1甲酸溶液的c(H+)约为1×10-2mol?L-1 | |
| B. | 甲酸能与活泼金属反应生成氢气 | |
| C. | 10 mL 1 mol?L-1甲酸恰好与10 mL 1 mol?L-1 NaOH溶液完全反应 | |
| D. | 在相同条件下,甲酸溶液的导电性比二元强酸溶液的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向用NaHSO4溶液中滴加Ba(OH)2至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| B. | NaHSO4为离子化合物在熔融状态下能导电:NaHSO4=Na++H++SO42- | |
| C. | FeCl3腐蚀铜制印刷电路板:Fe3++Cu=Fe2++Cu2+ | |
| D. | NH4Cl溶液显酸性是因为NH4+发生水解:NH4++2H2O?NH3•H2O+H3O+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com