

���� ��1�������ݵ�⾫����ԭ���Ǵ�ͭ����������ͭ����������ͭ���ӵĵ������Һ���е�ⷴӦ������������Һ��ͭ���ӵõ���������ͭ��
�����ݵ缫��Ӧ�����غ����׳غ��ҳ��е缫��������ʵ������ҳ������������Ӻ������������غ㣬ˮ�����ӻ���������õ���
��2���׳���ȼ�ϵ���У�ͨ�����ļ����������ü��Ϸ��������õ��ӵĻ�ԭ��Ӧ�������ܷ�Ӧ����ʽΪ��C2H5OH+3O2+4KOH=2K2CO3+5H2O���ҳ���������Ӧ��4OH--4e-�TO2��+2H2O��������Ӧ�����ǣ�Cu2++2e-�TCu��2H++2e-�TH2��
��� �⣺��1���ٵ�⾫����ԭ���Ǵ�ͭ����������ͭ����������ͭ���ӵĵ������Һ��CuSO4��Һ��CuCl2��Һ�����е�ⷴӦ������������Һ��ͭ���ӵõ���������ͭ���缫��Ӧ��Cu2++2e-�TCu��
�ʴ�Ϊ��Cu2++2e-�TCu��
�ڼ׳�AΪ���ص��������缫��ӦΪCu2++2e-�TCu������0.128g��ͭ���ʵ���Ϊ0.02mol��ת�Ƶ������ʵ���Ϊ0.04mol��
�ҳ�C��ʯī����Ϊ���ص��������缫��ӦΪ��2Cl--2e-�TCl2�������ݵ����غ㣬��������0.02mol���ų������ڱ���µ����Ϊ0.02mol��22.4L/mol=0.448L=448mL����ⱥ��ʳ��ˮ������2Cl-+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2OH-+H2��+Cl2����
�ʴ�Ϊ��2Cl--2e-�TCl2����448��2Cl-+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2OH-+H2��+Cl2����
��2���׳���ȼ�ϵ���У�ͨ�����ļ����������ҳ���������Ӧ��4OH--4e-�TO2��+2H2O����ȼ�ϵ���У��������Ҵ�ʧ���Ӻ����������ӷ�Ӧ����̼������Ӻ�ˮ���缫��ӦʽΪC2H5OH+16OH--12e-=2CO32-+11H2O��
�ʴ�Ϊ��4OH--4e-=2H2O+O2����C2H5OH+16OH--12e-=2CO32-+11H2O��
���� ���⿼����ԭ��ء�����ԭ�����Ȼ�ѧ��Ӧ����ʽ����д����ȷȼ�ϵ�����������жϷ������������ӷŵ�˳�ɽ���ѵ��ǵ缫��Ӧʽ����д���Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | S��s��+O2��g���TSO2��g����H=-296.8 kJ/mol����Ӧ�ȣ� | |
| B�� | NaOH��aq��+HCl��aq���TNaCl��aq��+H2O��l����H=+57.3 kJ/mol���к��ȣ� | |
| C�� | C2H5OH��l��+3O2��g���T2CO2��g��+3H2O��g����H=-1 367.0 kJ/mol��ȼ���ȣ� | |
| D�� | 2NO2�TO2+2NO��H=+116.2 kJ/mol����Ӧ�ȣ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
A�����ø�װ��ȷ��ȡ9.20ml������Һ | B����ϴ��Һת�Ƶ�����ƿ�У�Ӧ�ò�ȡ��ͼ�IJ���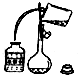 |
| C�����˺������ж���Ҫʹ�ò��������Ҳ���������;һ�� | D������NaOHӦʹ�ô���Ƥ���IJ����Լ�ƿ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Һ�У�K+��Ca2+��Cl2��Br-���Դ������� | |
| B�� | ��ʹ��I2�ĵ�����Һ��ɫ��ȥ��˵��NaHSO3��Һ��Ư���� | |
| C�� | ��FeCl3��Ӧ�����ӷ���ʽ��SO32-+2Fe3++H2O=SO42-+2Fe2++2H+ | |
| D�� | ������Ca��OH��2��Һ��Ӧ�����ӷ���ʽ��Ca2++OH-+HSO3-=CaSO3��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com