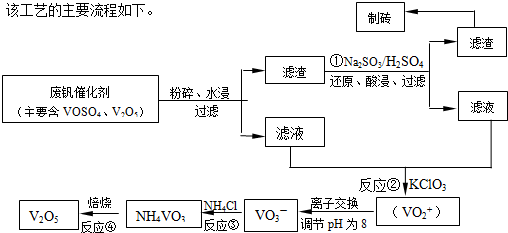
随着材料科学的发展,金属钒及其化合物得到了越来越广泛的应用,并被誉为“合金的维生素”.为回收利用含钒催化剂(含有V
2O
5、VOSO
4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,回收率达91.7%以上.
部分含钒物质在水中的溶解性如下表所示:
| 物质 |
VOSO4 |
V2O5 |
NH4VO3 |
(VO2)2SO4 |
| 溶解性 |
可溶 |
难溶 |
难溶 |
易溶 |

请回答下列问题:
(1)请写出加入Na
2SO
3溶液发生反应的离子方程式
V2O5+SO32-+4H+=2VO2++SO42-+2H2O
V2O5+SO32-+4H+=2VO2++SO42-+2H2O
.
(2)催化氧化所使用的催化剂钒触媒(V
2O
5)能加快二氧化硫氧化速率,此过程中产生了一连串的中间体(如下左图).

其中a、c二步的化学方程式可表示为
SO2+V2O5?SO3+V2O4
SO2+V2O5?SO3+V2O4
,
4VOSO4+O2?2V2O5+4SO3
4VOSO4+O2?2V2O5+4SO3
.
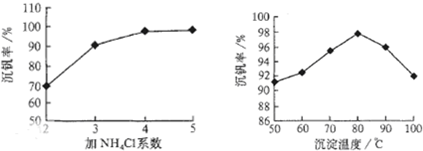
(3)该工艺中沉矾率是回收钒的关键之一,沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH
4Cl加入质量与料液中V
2O
5的质量比)和温度.
根据图试建议控制氯化铵系数和温度:
4
4
、
80℃
80℃
.
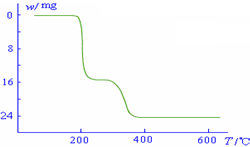
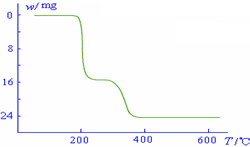
(4)经过热重分析测得:NH
4VO
3在焙烧过程中,固体质量的减少值(纵坐标)随温度变化的曲线如右图所示.
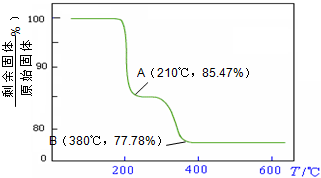
则NH
4VO
3在分解过程中
B
B
.
A.先分解失去H
2O,再分解失去NH
3B.先分解失去NH
3,再分解失去H
2O
C.同时分解失去H
2O和NH
3D.同时分解失去H
2、N
2和H
2O.




 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案
 其中a、c二步的化学方程式可表示为
其中a、c二步的化学方程式可表示为
 则NH4VO3在分解过程中
则NH4VO3在分解过程中

 化的曲线如右图所示.则NH4VO3在分解过程中
化的曲线如右图所示.则NH4VO3在分解过程中
 化的曲线如右图所示.则NH4VO3在分解过程中______.
化的曲线如右图所示.则NH4VO3在分解过程中______.