
| A. | 使品红溶液褪色 | B. | 使溴水褪色 | C. | 与氢硫酸反应 | D. | 与烧碱反应 |
分析 A、二氧化硫使品红溶液褪色是漂白性;
B、二氧化硫与溴水发生氧化还原反应而褪色;
C、二氧化硫与氢硫酸发生氧化还反应生成单质硫;
D、二氧化硫是酸性氧化物与氢氧化钠反应生成亚硫酸钠和水.
解答 解:A、二氧化硫使品红溶液褪色是漂白性,而不是二氧化硫的还原性的体现,故A错误;
B、二氧化硫与溴水发生氧化还原反应而褪色,生成硫酸,硫元素由+4价变+6价,化合价升高发生氧化反应,是还原剂、体现还原性,故B正确;
C、二氧化硫与氢硫酸发生氧化还反应生成单质硫,硫元素由+4价变0价,化合价降低发生还原反应,是氧化剂、体现氧化性,故C错误;
D、二氧化硫是酸性氧化物与氢氧化钠反应生成亚硫酸钠和水,非氧化还原反应,故D错误;
故选B.
点评 本题考查二氧化硫的性质,二氧化硫属于酸性氧化物、具有氧化性和还原性及漂白性,注意化合价的变化分析解答,题目难度不大.


 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 大量塑料废弃物会造成严重的白色污染,应将其焚烧处理 | |
| B. | 应用放射性同位素发射出的射线,可进行食物保鲜和肿瘤治疗 | |
| C. | 过度开采使用煤、石油等化石燃料,会导致空气中PM2.5浓度升高 | |
| D. | 近两年全国普遍取消了各种节日焰火晚会,对减缓空气污染起到了一定作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
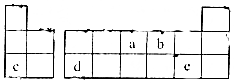
| A. | 气态氢化物的稳定性:a>b>c | |
| B. | 原子半径大小:a>b>c | |
| C. | c,d,e的氧化物对应的水化物之间两两皆能反应 | |
| D. | b、c形成的化合物中阴、阳离子的个数比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24 L C12与足量铁粉反应转移的电子数为0.2NA | |
| B. | 2 L 0.1 mol•L-1Na2CO3溶液中所含CO32-的数目为0.2NA | |
| C. | 28 g C2H4所含共用电子对数目为4NA | |
| D. | 1 mol H2O中所含的中子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
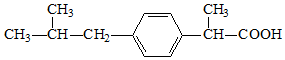
| A. | 布洛芬的分子式为C13H18O2 | |
| B. | 布洛芬与苯乙酸是同系物 | |
| C. | 1mol 布洛芬最多能与3mol 氢气发生加成反应 | |
| D. | 布洛芬在苯环上发生取代反应,其一氯代物有4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用加酶洗衣粉洗衣服时水的温度越高越好 | |
| B. | “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化物有关 | |
| C. | 小苏打是制作馒头的膨松剂,苏打是治疗胃酸过多的抗酸剂 | |
| D. | 乙醇、过氧化氢、次氯酸钠等消毒液的消毒原理都是利用其强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16 g O2和O3 的混合气体中含有的分子数为0.5 NA | |
| B. | 25℃时,Ksp(BaSO4)=1×10-10,则BaSO4饱和溶液中Ba2+数日为1×10-5 NA | |
| C. | 标准状况下,2.24 L Cl2 通入足量H2O或NaOH溶液中转移的电子数均为0.1 NA | |
| D. | 常温下,1 mol的NaHCO3固体中含HCO3-的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
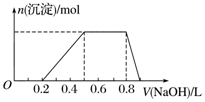
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com