
| A. | ①②③④⑤ | B. | 只有①④⑤ | C. | 只有②③ | D. | 只有③④ |
分析 ①少量Ca(OH)2投入过量NaHCO3溶液中发生复分解反应有碳酸钙是白色沉淀生成;
②过量NaOH溶液和明矾溶液混合,反应生成偏铝酸钠,无沉淀产生;
③钠和水反应生成的氢氧化钠和FeCl2溶液发生复分解反应生成Fe(OH)2,最终生成红褐色的Fe(OH)3;
④碳酸酸性比氢氧化铝强,过量CO2通入NaAlO2溶液中生成氢氧化铝白色沉淀;
⑤向饱和Na2CO3溶液中通入足量CO2会析出白色的碳酸氢钠晶体.
解答 解:①少量Ca(OH)2投入过量NaHCO3溶液中发生的反应为:Ca(OH)2+NaHCO3=CaCO3 ↓+H2O+NaOH,碳酸钙是白色沉淀,所以有白色沉淀生成,故正确;
②过量NaOH溶液和明矾溶液混合,发生的反应是:3OH+Al3+=Al(OH)3↓,AlOH3+OH-=AlO2-+2H2O,所以最终没有沉淀生成,故错误;
③金属钠投入到烧杯中的FeCl2溶液中,发生的反应为:2Na+2H2O=2NaOH+H2 ↑,2NaOH+FeCl2=Fe(OH)2 ↓+2NaCl,4Fe(OH)2+O2+2H2O=4Fe(OH)3,所以最终生成的沉淀是红褐色的,所以不符合,故错误;
④向NaAlO2溶液中通入过量CO2溶液发生的反应为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,氢氧化铝是白色沉淀,故正确;
⑤向饱和Na2CO3溶液中通入足量CO2发生的反应为:Na2CO3+H2O+CO2=2NaHCO3,碳酸氢钠的溶解性小于碳酸钠的溶解性,所以向饱和Na2CO3溶液中通入足量CO2会析出碳酸氢钠晶体,所以产生白色沉淀,故正确;
故选B.
点评 本题考查物质之间的化学反应,为高频考点,侧重于学生的分析能力的考查,熟悉复分解反应发生的条件及常见物质的溶解性是解答本题的关键,注意⑤根据物质的溶解度能判断产生沉淀,该题为易错选项.


科目:高中化学 来源: 题型:解答题
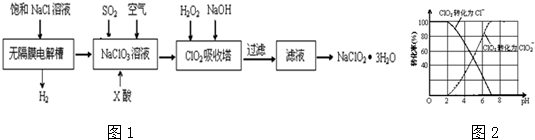
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
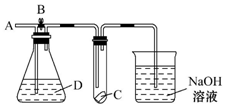 如图所示,A处通入干燥的Cl2,打开B阀后,C处的红布条逐渐褪色,关闭B阀时,C处的红布条看不到明显现象,则D瓶中装的是( )
如图所示,A处通入干燥的Cl2,打开B阀后,C处的红布条逐渐褪色,关闭B阀时,C处的红布条看不到明显现象,则D瓶中装的是( )| A. | 浓硫酸 | B. | NaOH溶液 | C. | 浓盐酸 | D. | 饱和NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
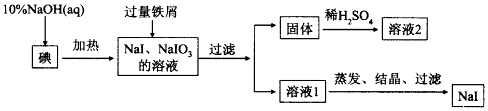
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分离对硝基甲苯和邻硝基甲苯:蒸馏 | |
| B. | 除去甲基丙烯酸甲酯中少量甲醇:蒸馏 | |
| C. | 除去漠苯中少量水:分液 | |
| D. | 从粗产品中提纯苯甲酸钠:重结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2在反应中只作氧化剂 | |
| B. | 由于Na2O2与H2O反应放出热量和氧气,所以脱脂棉剧烈燃烧 | |
| C. | Na2O2与H2O反应中有氢氧化钠生成,Na2O2是典型的碱性氧化性 | |
| D. | Na2O2与H2O反应中有氧气生成,可用于防毒面具上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.1 g | B. | 10.2 g | C. | 13.6 g | D. | 15.3 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com