
| A. | AgCl沉淀多于AgBr沉淀 | B. | AgCl和AgBr沉淀等量生成 | ||
| C. | AgCl沉淀少于AgBr沉淀 | D. | 只有AgBr沉淀生成 |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
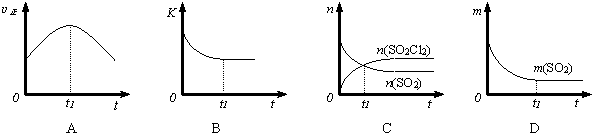
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 观察两者的颜色 | B. | 观察两者的状态 | ||
| C. | 通入溴的四氯化碳溶液 | D. | 通入高锰酸钾酸性溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④ | C. | ①④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 棉花、羊毛及合成纤维完全燃烧都只生成二氧化碳和水 | |
| B. | 淀粉、油脂、蛋白质都能发生水解反应,都属于天然有机高分子化合物 | |
| C. | 蛋白质遇饱和硫酸铵溶液产生的沉淀能重新溶于水 | |
| D. | 苯和乙烯都能使溴水褪色,均与溴发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此回答:
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状态下的辛烷22.4L完全燃烧产生CO2分子数为8NA | |
| B. | 18克水所含的电子数为10NA | |
| C. | 46克NO2和46克N2O4中所含原子数均为3NA | |
| D. | 1L2molL的Mg(NO3)2溶液中含NO3个数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 设锌镀层厚度为h,锌的密度为ρ,则$\frac{{{m_1}-{m_2}}}{ρS}$=h | |
| B. | 锌电极上发生还原反应 | |
| C. | 锌和石墨形成原电池,外电路中电流从锌流向石墨 | |
| D. | 当石墨不再产生气泡时,应立即取出铁皮 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com