

分析 (1)平衡常数指产物浓度系数次幂的乘积与反应物浓度系数次幂的乘积的比值;
(2)根据图1分析,温度越高,甲烷越少,说明平衡正向移动;平衡常数仅与温度有关,据此分析;
(3)根据图1分析,温度越高,甲烷越少,图2分析,压强越高,甲烷越多,据此分析;
(4)工业生产中使用镍作催化剂.但要求原料中含硫量小于5×10-7%,防止催化剂中毒,失去催化效果.
解答 解:(1)平衡常数指产物浓度系数次幂的乘积与反应物浓度系数次幂的乘积的比值,所以反应CH4(g)+H2O(g)?CO(g)+3H2(g)的平衡常数k=$\frac{c(CO)•c{\;}^{3}(H{\;}_{2})}{c(CH{\;}_{4})•c(H{\;}_{2}O)}$,故答案为:$\frac{c(CO)•c{\;}^{3}(H{\;}_{2})}{c(CH{\;}_{4})•c(H{\;}_{2}O)}$;
(2)根据图1分析,温度越高,甲烷越少,说明平衡正向移动,则升高温度,平衡常数K增大,又平衡常数仅与温度有关,所以降低反应的水碳比,平衡常数K不变,故答案为:增大;不变;
(3)根据图1分析,温度越高,甲烷越少,所以t1<t2;图2分析,压强越高,甲烷越多,所以当压强为2MPa时,CH4平衡含量与水碳比之间关系曲线应该是a;故答案为:<;a;
(4)工业生产中使用镍作催化剂.但要求原料中含硫量小于5×10-7%,防止催化剂中毒,失去催化效果,故答案为:防止催化剂中毒,失去催化效果.
点评 本题考查了平衡常数的表达式的书写以及影响因素,图象分析,平衡常数概念的分析应用是解题关键,题目难度中等.


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:解答题
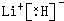 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙溶于醋酸CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 锌片插入硝酸银溶液中Zn+Ag+═Zn2++Ag | |
| C. | 在稀氨水中通入过量CO2:NH3•H2O+CO2═NH4++HCO3- | |
| D. | 硫酸镁溶液和氢氧化钡溶液反应 SO42-+Ba2+═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 位于短周期的X元素的阳离子与Y元素的阴离子具有相同的电子层结构,则两元素的最高正化合价一定是X<Y | |
| B. | 对于某元素的单质,若它的氧化性弱,那么它的还原性一定强 | |
| C. | 热稳定性:AsH3<PH3<H2O<HF | |
| D. | 最外层电子数较少的金属元素,一定比最外层电子数较多的金属元素活泼性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| I | Ii | Iii | |
| 备选装置 |  |  |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 天然橡胶 和杜仲胶 和杜仲胶 属于同分异构体 属于同分异构体 | |
| B. |  属于同系物 属于同系物 | |
| C. | 合成 的单体为乙烯和2-丁烯 的单体为乙烯和2-丁烯 | |
| D. |  是由苯酚和甲醛发生加成反应后的产物脱水缩合而成 是由苯酚和甲醛发生加成反应后的产物脱水缩合而成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
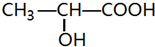 有机物甲的结构简式如图所示,利用该物质为原料制成的高分子材料乙具有生物兼容性.下列关于甲、乙的判断,错误的是( )
有机物甲的结构简式如图所示,利用该物质为原料制成的高分子材料乙具有生物兼容性.下列关于甲、乙的判断,错误的是( )| A. | 甲能与碳酸氢钠溶液发生反应 | |
| B. | 1mol甲能与2molNaOH反应 | |
| C. | 一定条件下,甲可发生酯化反应 | |
| D. | 由甲为原料制成高分子材料乙的反应不是加聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用潮汐能电解水制氢气 | B. | 大力推广乙醇汽油燃料汽车 | ||
| C. | 利用甲烷制造燃料电池 | D. | 提倡化石燃料燃烧 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com