
| A. | 用铁做阳极材料电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ | |
| B. | 碱性甲烷燃料电池的负极反应式:CH3OH-6e-+6OH-═CO2+5H2O | |
| C. | 粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-═Cu2+ | |
| D. | 钢铁发生电化学腐蚀的负极反应式:Fe-2e-→Fe2+ |
分析 A.活性电极作阳极,电极失电子;
B.碱性甲烷燃料电池中,负极上燃料失电子和氢氧根离子反应生成碳酸根离子和水;
C.电解精炼铜时,粗铜作阳极;
D.钢铁发生电化学腐蚀时,负极上铁失电子发生氧化反应.
解答 解:A.用铁做阳极材料电解饱和食盐水时,阳极上Fe失电子生成亚铁离子,电极反应式为Fe-2e-═Fe2+,故A错误;
B.碱性甲烷燃料电池中,负极上燃料失电子和氢氧根离子反应生成碳酸根离子和水,负极反应式:CH3OH-6e-+8OH-═CO32-+6H2O,故B错误;
C.电解精炼铜时,粗铜作阳极,则电源正极相连的是粗铜,电极反应式为:Cu-2e-═Cu2+,故C错误;
D.钢铁发生电化学腐蚀时,负极上铁失电子发生氧化反应,电极反应式为Fe-2e-═Fe2+,故D正确;
故选D.
点评 本题考查电极反应式的书写,题目难度不大,明确各个电极上发生的反应是解本题关键,书写电极反应式要结合电解质溶液酸碱性,也是学习难点.


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | NaNO2发生的是氧化反应 | B. | 生成1molN2时转移的电子数为3mol | ||
| C. | NH4Cl中的N元素被还原 | D. | N2既是氧化剂有事还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 植树造林,加强绿化 | B. | 合理使用化肥和农药 | ||
| C. | 工业“三废”经处理后再排放 | D. | 矿物产品的综合开发和利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强电解质:盐酸、氢氧化钡、明矾 | |
| B. | 纯净物:冰水混合物;含氧40%的氧化镁 | |
| C. | 有单质参加和单质生成的化学反应一定是氧化还原反应 | |
| D. | 同位素:H2、D2、T2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
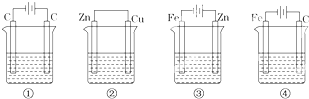
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| 选项 | M | N | P |
| A | NH3•H2O | Ba(OH)2 | Cu |
| B | Na | BaCl2 | FeO |
| C | NaOH | Ba(NO3)2 | Fe |
| D | Na2O | MgCl2 | Fe |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Mg2+、OH-、NO3- | B. | Al3+、NH4+、Br-、Cl- | ||
| C. | K+、HCO3-、Ca2+、SO42- | D. | Na+、K+、SiO32-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 摩尔质量/(g•mol-1) | 熔点/℃ | 沸点/℃ |
| Sn | 119 | 232 | 2260 |
| SnCl2 | 190 | 246.8 | 623 |
| SnCl4 | 261 | -30.2 | 114.1 |
| MnO2 | 87 | 535(分解) | - |
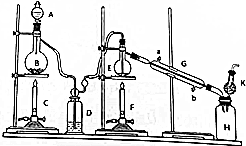
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com