
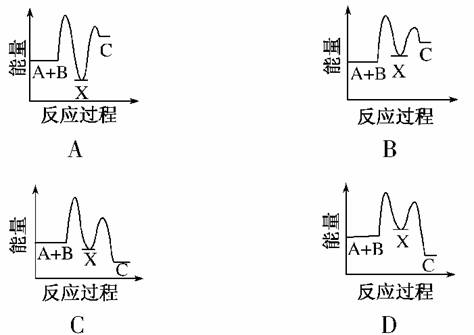
反应A+B—→C(ΔH<0)分两步进行:
①A+B—→X(ΔH>0),②X—→C(ΔH<0)。
下列示意图中,能正确表示总反应过程中能量变化的是( )
科目:高中化学 来源: 题型:
单质X和Y相互反应生成X2+和Y2-,现有下列叙述:
(a)X被氧化 (b)X是氧化剂
(c)X具有氧化性 (d)Y2-是还原产物
(e)Y2-具有还原性 (f) X2+具有氧化性
其中正确的是( )
A.(a)(b)(c)(d) B.(b)(c)(d)
C.(a)(d)(e)(f) D.(a)(c)(d)(e)
查看答案和解析>>
科目:高中化学 来源: 题型:
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变为H2、CO。其过程如下:
mCeO2太阳能①(m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xH2O+xCO2900 ℃②mCeO2+xH2+xCO
下列说法不正确的是( )
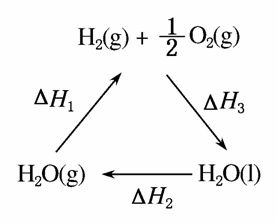
A.该过程中CeO2没有消耗
B.该过程实现了太阳能向化学能的转化
C.右图中ΔH1=ΔH2+ΔH3
D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH--2e-===CO+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
在火星上工作的美国“勇气号”、“机遇号”探测车的一个重要任务就是收集有关Fe2O3及硫酸盐信息,以证明火星上存在或曾经存在过水。以下叙述正确的是( )
A.铝热反应就是单指Fe2O3粉和Al粉的反应
B.检验从火星上带回来的红色物质是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液
C.分别还原a mol Fe2O3所需H2、Al、CO的物质的量之比为3:2:3
D.明矾属硫酸盐,含结晶水是混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学小组欲探究铁及其化合物的氧化性和还原性,请回答下列问题:
(1)除胶头滴管外,你认为本实验必不可缺少的一种玻璃仪器是__________。
(2)请帮他们完成以下实验报告:
实验目的:探究铁及其化合物的氧化性和还原性。
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片。
实验记录(画斜线部分不必填写,其他空格均应填充):
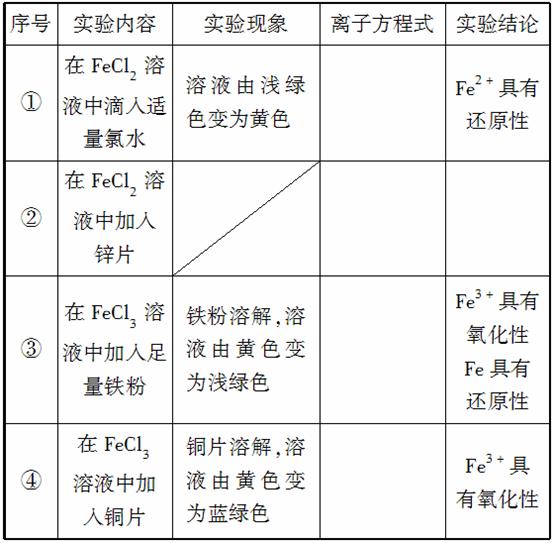
实验结论:Fe只有还原性,Fe3+只有氧化性,Fe2+既有氧化性,又有还原性。
(3)根据以上结论分析判断,下列物质中既有氧化性,又有还原性的有______________。
A.Cl2 B.Na C.Na+ D.Cl- E.SO2 F.NO2
(4)亚铁盐溶液在空气中易被氧化,实验室中应该加入__________防止亚铁盐被氧化。
查看答案和解析>>
科目:高中化学 来源: 题型:
用CH4催化还原NOx可以消除氮氧化物的污染。已知CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1,CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH=-1 160 kJ·mol-1。若在标准状况下4.48 L CH4恰好能将一定量NO2还原成N2和H2O(g),则整个过程中放出的热量为( )
A.114.8 kJ B.232 kJ
C.368.8 kJ D.173.4 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
十七大报告指出,应加强能源资源节约和生态环境保护,增强可持续发展能力。下列行为与之不相符的是
A.大量使用化学肥料,提高农作物的产量和质量
B.将作物秸秆通过化学反应转化为乙醇用作汽车燃料
C.使用资源节约型、环境友好型的生物降解塑料包装
D.推广煤炭脱硫技术、减少直接燃煤,防止酸雨发生
查看答案和解析>>
科目:高中化学 来源: 题型:
Q、W、X、Y、Z五种短周期元素,原子序数依次增大。Q在元素周期表中原子半径最小,W元素最高正价与最低负价代数和为0;Y与Q同主族;X、Z分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)X、Z简单离子半径较大是 (用离子符号表示)。
(2)由这五种元素中的若干种组成的化合物甲、乙、丙、丁在水溶液中有如下转化关系:
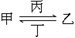
其中丙是溶于水显酸性的气体,丁是强碱。
①若乙常作为焙制糕点的发酵粉,则乙含有的化学键类型有 。
②若乙是难溶物,甲溶液与过量的丙生成乙的离子方程式为:
。
查看答案和解析>>
科目:高中化学 来源: 题型:
氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用。回答下列问题:
(1)氮元素原子的L层电子数为______;
(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为_________;
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)====N2O4(l) ΔH1=-19.5 kJ·mol-1
②N2H4(l)+O2(g)====N2(g)+2H2O(g) ΔH2=-534.2 kJ·mol-1
写出肼和N2O4反应的热化学方程式____________;
(4)肼——空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为___
______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com