
【题目】固体氧化物燃料电池是以固体氧化锆﹣氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2﹣)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应,下列判断正确的是( ) 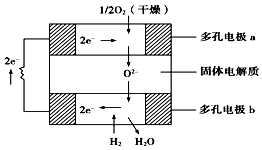
A.有O2参加反应的a极为电池的负极
B.b极的电极反应式为H2+O2﹣﹣2e﹣═H2O
C.a极对应的电极反应式为O2+2H2O+4e﹣═4OH﹣
D.氧化锆的作用是让电子在电池内部通过
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是( )
A. 乙烯、聚乙烯和苯分子中均含有碳碳双键
B. 苯、油脂均不能使酸性高锰酸钾溶液褪色
C. 乙醇、乙酸均能与Na反应放出H2,二者分子中官能团相同
D. 甲烷和Cl2的反应与乙烯和Br2的反应不属于同一类型的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到目的的是( )
A. 用溴水鉴别苯和正己烷
B. 用BaCl2溶液鉴别SO42-与SO32-
C. 用浓HNO3与Cu反应制备NO2
D. 将混有HCl的Cl2通入饱和NaHCO3溶液中除去HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸钠﹣过氧化氢加合物(xNa2SO4yH2O2zH2O)的组成可通过下列实验测定:①准确称取1.7700g样品,配制成100.00mL溶液A.②准确量取25.00mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体0.5825g.③准确量取25.00mL溶液A,加适量稀硫酸酸化后,用0.02000molL﹣1KMnO4溶液滴定至终点,消耗KMnO4溶液25.00mL.H2O2与KMnO4反应的离子方程式如下:2MnO4﹣+5H2O2+6H+=2Mn2++8H2O+5O2↑
(1)已知室温下BaSO4的Ksp=1.1×10﹣10 , 欲使溶液中c(SO42﹣)≤1.0×10﹣6 molL﹣1 , 应保持溶液中c(Ba2+)≥molL﹣1 .
(2)上述滴定若不加稀硫酸酸化,MnO4﹣被还原为MnO2 , 其离子方程式为
(3)上述滴定到达终点的现象为
(4)通过计算确定样品的组成(写出计算过程).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000mol/L NaOH溶液滴定 20.00mL 0.1000 mol/L
CH3COOH溶液滴定曲线如右图。下列说法正确的是
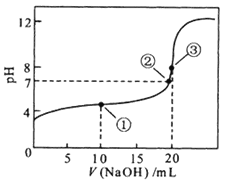
A. 点①所示溶液中:c(CH3COO-)+ c(OH-) =c(CH3COOH)+ c(H+)
B. 点②所示溶液中:c(Na+) =c(CH3COOH)+ c(CH3COO-)
C. 点③所示溶液中:c(Na+)> c(OH-)> c(CH3COO-)> c(H+)
D. 滴定过程中可能出现:c(CH3COOH)> c(CH3COO-)> c(H+)> c(Na+)> c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种食用精制盐包装袋上有如表说明:
产品标准 | GB5461 |
产品等级 | 一级 |
配 料 | 食盐、碘酸钾、抗结剂 |
碘含量(以I计) | 20~50mg/kg |
分装时期 | |
分装企业 |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)KIO3+KI+H2SO4═K2SO4+I2+H2O
(2)上述反应生成的I2可用四氯化碳检验.向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳.
①Na2SO3稀溶液与I2反应的离子方程式是 .
②某学生设计回收四氯化碳的操作为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体d.将分液漏斗充分振荡后静置
其中分液漏斗使用前须进行的操作是 , 上述操作正确的顺序是:(填序号)
(3)已知:I2+2S2O32﹣═2I﹣+S4O62﹣ . 某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10﹣3molL﹣1的Na2S2O3溶液10.0mL,恰好反应完全.
①判断c中反应恰好完全依据的现象是 .
②b中反应所产生的I2的物质的量是mol.
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)mg/kg.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氮气的叙述不正确的是
A.氮分子为非极性分子
B.在灯泡中充入氮气可防止钨丝被氧化
C.氮元素比磷元素非金属性强,所以硝酸比磷酸酸性强
D.氮分子中有2个σ键1个π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列金属冶炼的反应原理错误的是
A. 2NaCl(熔融)=== 2Na+Cl2↑B. Al2O3+ 3H2 ===2Al + 3H2O
C. Fe2O3 + 3CO === 2Fe + 3CO2D. ZnO + CO === Zn + CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计一个燃料电池(如下图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
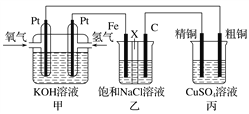
根据要求回答相关问题:
(1)通入氢气的电极为________(填“正极”或“负极”),负极的电极反应式为__________。
(2)石墨电极为________(填“阳极”或“阴极”),反应一段时间后,在乙装置中滴入酚酞溶液,________(填“铁极”或“石墨极”)区的溶液先变红。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将________(填“增大”“减小”或“不变”)。精铜电极上的电极反应式为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com