
����Ŀ��������ˮ�п��ܴ��ڵ���ƽ�⡢�ε�ˮ��ƽ��ͳ������ܽ�ƽ�⣬���Ƕ��ɿ�����ѧƽ�⡣�������ѧ��֪ʶ�ش�
��1��0.1 mol��L��1��NH4Cl��Һ���ڸ���Һ�и������ӵ�Ũ���ɴ�С˳��Ϊ_________��
��2��0.1 mol��L��1 NaHCO3��Һ�������NaHCO3��Һ�Լ��Ե�ԭ��________��
��3��FeCl3��Һ��ʵ����������FeCl3��Һʱ������____________��������ˮ�⡣
��4������AgI����ı�����Һ�У�
�ټ������AgNO3����c(I��)_____(������ ��С�����䡱����ͬ)��c(Ag��)__��
�����ļӸ����AgI����c(Ag��)��____��
�����ļ�Na2S���壬��c(I��)____��c(Ag��)_____��
���𰸡�c(Cl-)>c(NH4+)> c(H+)>c(OH-) HCO3-��ˮ�����HCO3-�ĵ��� HCl ��С ��� ���� ��� ��С
��������
��1���Ȼ����Һ��笠���������ˮ�⣬ʹ��Һ�������ԣ�
��2��HCO3������ˮ��ƽ��͵���ƽ�⣬��ˮ��ƽ��Ϊ����
��3��FeCl3��Һ�У�����������ˮ��ʹ��Һ�����ԣ�
��4�����ݳ����ܽ�ƽ����ƶ����͡�
(1) 0.1 mol��L��1��NH4Cl��Һ��笠���������ˮ��,ˮ�����ӷ���ʽΪNH4++H2O![]() NH3H2O+H+����Һ�е�����Ũ�ȴ�СΪ: c(Cl-)>c(NH4+)> c(H+)>c(OH-)��
NH3H2O+H+����Һ�е�����Ũ�ȴ�СΪ: c(Cl-)>c(NH4+)> c(H+)>c(OH-)��
��: c(Cl-)>c(NH4+)> c(H+)>c(OH-)
(2) 0.1 mol��L��1 NaHCO3��Һ�д���̼��������ӵ�ˮ��ƽ��Ϊ:HCO3��+H2O![]() H2CO3+OH��,����ƽ��Ϊ: HCO3��
H2CO3+OH��,����ƽ��Ϊ: HCO3��![]() CO32-+H+��HCO3����ˮ��̶ȴ��ڵ���̶���Һ,���Լ��ԣ�
CO32-+H+��HCO3����ˮ��̶ȴ��ڵ���̶���Һ,���Լ��ԣ�
�𰸣�HCO3-��ˮ�����HCO3-�ĵ���
(3)ʵ����������FeCl3��Һʱͨ����Ҫ�����м���������Fe3+ˮ�⣻
�𰸣�HCl
��4��������AgI����ı�����Һ�д���AgI��s��![]() Ag+��aq��+I-��aq���У��������AgNO3��������c��Ag+����ƽ�������ƶ�����c(I��) ��С��c(Ag��)��δ����AgNO3ʱ���
Ag+��aq��+I-��aq���У��������AgNO3��������c��Ag+����ƽ�������ƶ�����c(I��) ��С��c(Ag��)��δ����AgNO3ʱ���
�𰸣���С ���
������AgI����ı�����Һ�У����ļӸ����AgI����Ϊ�¶�һ��ʱ������AgI��Һ�У�����Ũ��һ����c(Ag��)�����䣻
�𰸣�����
������AgI����ı�����Һ�д���AgI��s��![]() Ag+��aq��+I����aq���У��ļ�Na2S���壬ӦΪAg+��S2-��Ӧ����Ag2S�����������ܽ�ƽ�������ƶ�����c(I��)���c(Ag��)��С��
Ag+��aq��+I����aq���У��ļ�Na2S���壬ӦΪAg+��S2-��Ӧ����Ag2S�����������ܽ�ƽ�������ƶ�����c(I��)���c(Ag��)��С��
�𰸣���� ��С



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�̶ֹ�������CO2�Ĺ����������£�
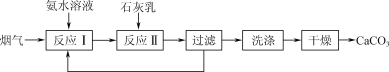
(1) ����Ӧ���У�CO2�������ˮ��Ӧ�����ӷ���ʽΪ________��
(2) ����Ӧ���У����������CO2ȥ���ʵĿ��д�ʩ��________(����ĸ)��
a. ���ø��¡���������b. �ӿ��������١�����������c. ����ˮŨ��
(3) �������Һ��c(CO32-)��10��2 mol��L��1����Ca2���Ƿ������ȫ��________(����������������)��[c(Ca2��)<10��5 mol��L��1ʱ��Ϊ������ȫ��Ksp(CaCO3)��4.96��10��9]
(4) ����Ӧ���У���Һ��pH�͵��������仯��ͼ1��ʾ������������ʼʱ���ٽ��ͣ�������������ԭ����____________________________________________��
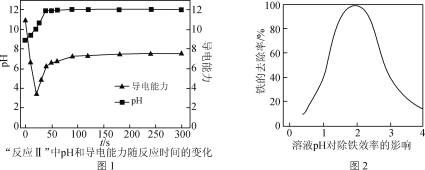
(5) CaCO3�����ڵ��ڷ�ˮ��pH���Գ�ȥ���е�Fe3������ҺpH�Գ���Ч��Ӱ����ͼ2��ʾ��
�ٳ���ʱӦ������Һ��pHΪ________(����ĸ)��
a. 0.5��1.5��������������b. 1.5��2.5��������������c. 2.5��3.5
�� ����ʱpH�Դ������Fe(OH)3���壬�������ͳ���Ч�ʣ���ԭ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X(g)+3Y(g) ![]() 2Z(g) ��H=��a kJ��mol��1 ��һ�������£���1 mol X��3 mol Yͨ��2L�ĺ����ܱ������У���Ӧ10min�����Y�����ʵ���Ϊ2.4 mol������˵����ȷ����( )
2Z(g) ��H=��a kJ��mol��1 ��һ�������£���1 mol X��3 mol Yͨ��2L�ĺ����ܱ������У���Ӧ10min�����Y�����ʵ���Ϊ2.4 mol������˵����ȷ����( )
A.10min�ڣ�����0.2 mol X������0.4 mol Z
B.��10minʱ��X�ķ�Ӧ����Ϊ0.01 mol��L��1��min��1
C.10min�ڣ�Y��ƽ����Ӧ����Ϊ0.03 mol��L��1��s��1
D.10min�ڣ�X��Y��Ӧ�ų�������Ϊa kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯��ͼ��ʾ����֪W��һ�ֺ��ص�������Ϊ14��������Ϊ7��X��������NH4+������ͬ�����ӡ�������Ŀ��W��Y����������ܵ���������γɣ�Z�ķǽ�������ͬ��������Ԫ������ǿ��
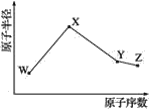
��1��Y�����ڱ��е�λ����__��
��2��X3W��ˮ���ͷų�ʹ��̪��Һ��������A����ѧ����ʽ��__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�����⼼��ԭ����ͼ��ʾ������˵����ȷ���ǣ� ��
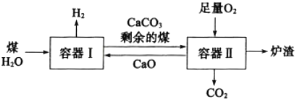
A.���������м���CaO����Чʵ��H2��CO2�ķ���
B.��Ϊ�������л���ʣ���ú�������ж�ú��H2O�ķ�ӦΪ���淴Ӧ
C.ʣ���ú������������������O2��Ӧ�ų��������ֽ�CaCO3
D.ú�к��е���Ԫ����������������ת��ΪCaSO3����¯��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ���仯�������������������Ź㷺��Ӧ�á���ش��������⣺
(1)ͭԪ��λ��Ԫ�����ڱ���_____������̬Cuԭ����______�ֲ�ͬ�ܼ��ĵ��ӡ�
(2)ͭ�Ͻ���������캽ĸ����������������в����ĺ�ͭ��Һ������ͭ��ȡ��M��ͨ�����·�Ӧʵ��ͭ���ӵĸ������ա�
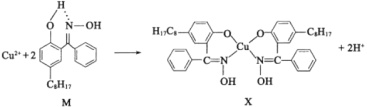
��M����Ԫ�صĵ縺���ɴ�С��˳��Ϊ______(��Ԫ�ط��ű�ʾ)��
��X�в���sp3�ӻ��ķǽ���ԭ����______(��Ԫ������)��
(3)�ڽϵ��¶���CuFeS2��Ũ��������ʱ����������������ζ������Y������Y���ӵ����幹����_______��Y�ķе��ˮ�͵���Ҫԭ����_______��
(4)����ɫ{[Cu(H2O)4]2+}����ͭ��Һ�м����Թ����İ�ˮ����Һ��Ϊ����ɫ{[Cu(NH3)4]2+}��ͨ������ʵ�������֪����Cu2+����λ������H2O________NH3(����ڡ���С�ڡ�)��
(5)CuCl2��CuCl��ͭ�������Ȼ��
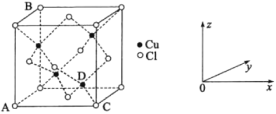
��ͼ�б�ʾ����_______(�CuCl2����CuCl��)�ľ�����
��ԭ�����������������ʾ�����ڸ�ԭ�ӵ����λ�ã�ͼ�и�ԭ���������AΪ(0��0��0)��BΪ(0��1��1)��CΪ(1��0��0)����Dԭ�ӵ��������Ϊ______��
�۾�����C��D��ԭ�Ӻ˼��Ϊ298 pm�������ӵ�������ֵΪNA����þ����ܶ�Ϊ__g��cm-3(�г�����ʽ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ�ܿ���Ҫ�ɷ�ΪCo2O3��������Fe2O3��Al2O3��MnO��MgO��CaO��SiO2�ȣ�������ȡ���ֻ����Լ�������Ϊ�����ܾ�����Ȼ��ܾ�����Ʊ����̣��ش��������⣺
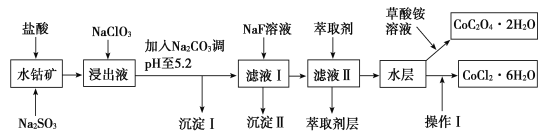
��֪���ٽ���Һ�к��е���������Ҫ��H+��Co2+��Fe2+��Mn2+��Al3+��Mg2+��Ca2+�ȡ�
�ڳ�������ֻ�������ֳ�����
�������в���������������������ʽ����ʱ��Һ��pH������
������ | ��ʼ���� | ��ȫ���� |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.6 |
Co(OH)2 | 7.6 | 9.2 |
Al(OH)3 | 4.0 | 5.2 |
Mn(OH)2 | 7.7 | 9.8 |
��1�������������������뻹ԭ�����ʵ���֮��Ϊ___��
��2��NaClO3�ڽ���Һ�з�����Ӧ�����ӷ���ʽΪ___��
��3������Na2CO3��pH��5.2��Ŀ����___����ȡ���㺬��Ԫ�أ�����������Ҫ�ɷ�Ϊ__��
��4���������������ˮ�����Ũ�������pHΪ2��3��___��___�����ˡ�ϴ�ӡ���ѹ��ɵȹ��̡�
��5��Ϊ�ⶨ�ֲ�Ʒ��CoCl2��6H2O�ĺ�������ȡһ�������Ĵֲ�Ʒ����ˮ���������������ữ����������Һ�����ˡ�ϴ�ӡ���������������ͨ�����㷢�ֲִ�Ʒ��CoCl2��6H2O������������100%����ԭ�������___���ش�һ��ԭ�ɣ���
��6����5.49g�����ܾ���(CoC2O4��2H2O)���ڿ����м��ȣ����ȹ����в�ͬ�¶ȷ�Χ�ڷֱ�õ�һ�ֹ������ʣ������������
�¶ȷ�Χ/�� | 150��210 | 290��320 |
��������/g | 4.41 | 2.41 |
���ⶨ���������ȹ��̣�ֻ����ˮ������CO2���壬��290��320���¶ȷ�Χ��ʣ��Ĺ������ʻ�ѧʽΪ___��[��֪��CoC2O4��2H2O��Ħ������Ϊ183g��mol-1]
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Cl2��Ca(OH)2�Ʊ�����Ư�۾���һ�ֺ�������������װ�����¡�
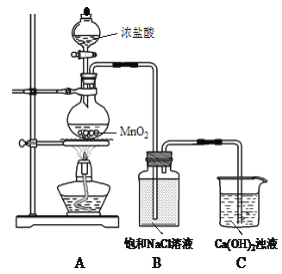
��1��AΪ��������װ�á�A�з�Ӧ����ʽ��________��
��2��B�����������ջӷ�����HCl��HCl���ܶ��Ʊ�Ư�۾���ɵ�Ӱ����________��
��3����Cl2��Ca(OH)2�Ʊ���Ư�۾�������Ч�ɷ���_________��
��4��Ư�۾���������Ӿ�ص����������������õ���HClO��Ư�۾���ˮ���ͷ�HClO��;�����£�
;��һ��Ca(ClO)2 + 2H2O Ca(OH)2 + 2HClO
;������Ca(ClO)2 + H2O + CO2 ��________+ _______���ѷ�Ӧ����������
��5����ˮ������Զ�Ư�۾�������Ч��Ӱ�����ԡ�
�ٳ�ˮ���Թ�ǿ��ɱ�����û�________��������ǿ����������������
�ڳ�ˮ���Թ�ǿ����̼��۾���Ƥ����ͨ������Na2CO3��NaHCO3�Խ������ԣ������������õ����ӷֱ���________�������ӷ��ţ���
��6��ij����˻��ڼ䣬������������Ӿ��ˮ���̵��¼�����Ϊ��ʱ��һ�����š��йظ�
����˵����ˮ����������������ɵġ�����Ӿ��ÿ��һ��ʱ���ҪͶ�ź��������������ٴ�Ͷ��ʱ����Ͷ�˹������⣨H2O2����������������Ϊʲô���������ˣ�_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ĸ���ͬ�������У��ڲ�ͬ�������½��кϳɰ��ķ�Ӧ��������������ͬʱ���ڲⶨ�Ľ���жϣ���ѧ��Ӧ����������� �� ��
A.v(H2)=0.2 mol��L-1��min-1B.v(H2)=0.04 mol��L-1��s-1
C.v(N2)=0.01 mol��L-1��s-1D.v(N2)=0.2 mol��L-1��min-1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com