
⑴配位化学创始人维尔纳发现,将等物质的量的CoCl3?6NH3(黄色)、CoCl3?5NH3(紫红色)、CoCl3?4NH3(绿色)和CoCl3?4NH3(紫色)四种化合物溶于水,加入足量硝酸银溶液,立即产生氯化银沉淀的量分别为3mol、2mol、1mol和1mol。
①请根据实验事实用配合物的形式写出它们的化学式。
CoCl3?6NH3 CoCl3?5NH3
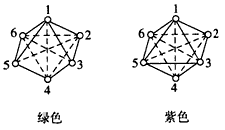
CoCl3?4NH3(绿色和紫色):
②后两种物质组成相同而颜色不同的原因是
③上述配合物中,中心离子的配位数都是
⑵向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成血红色。该反应在有的教材中用方程式FeCl3+3KSCN=Fe(SCN)3+3KCl表示。经研究表明,Fe(KSCN)3是配合物,Fe3+与SCN―不仅能以1∶3的个数比配合,还可以其他个数比配合。请按要求填空:
①Fe3+与SCN―反应时,Fe3+提供 、SCN―提供 ,二者通过配位键结合。
②所得Fe3+与SCN―的配合物中,主要是Fe3+与SCN―以个数比1∶1配合所得离子显血红色。含该离子的配合物的化学式是 。
③若 Fe3+与SCN―以个数比1∶5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为 。
④已知SCN―离子中所有原子均满足最外层8电子结构,一个电子是由S原子所得,则SCN―的电子式是 。
⑴①Co(NH3)6]Cl3;[Co(NH3)5Cl]Cl2;[Co(NH3)4Cl2]Cl;②它们互为同分异构体;③ 6;⑵①空轨道;孤电子对;②[Fe(SCN)]Cl2③FeCl3+5KSCN=K2[Fe(SCN)5]+3KCl;④![]() 。
。
错解分析:本题易错点在于一是不清楚配合物的组成而无法完成⑴、⑵小问,不熟悉原子原子的成键原则而无法正确书写出SCN―离子的电子式。
解题指导:⑴等物质的量的CoCl3?6NH3、CoCl3?5NH3、CoCl3?4NH3与足量的AgNO3反应分别生成3mol、2mol、1mol AgCl沉淀,说明它们能电离出的Cl分别为3mol、2mol、1mol,CoCl3?6NH3结构中配位体为NH3,CoCl3?5NH3、CoCl3?4NH3配位体为NH3和Cl,再根据化合价代数和等于零的原则即可写出相应的化学式分别为[Co(NH3)6]Cl3、[Co(NH3)5Cl]Cl2、[Co(NH3)4Cl2]Cl。中心离子的配位数分别为6、5+1=6、4+2=6。⑵CoCl3?4NH3(绿色)和CoCl3?4NH3(紫色)的化学式均为[Co(NH3)4Cl2]Cl,造成其颜色不同的原因在于它们存在同分异构体。⑶①Fe3+ 的核外电子排布为1s22s22p63s23p63d5,Fe3+具有空轨道,SCN―具有孤对电子,故二者通过配位键结合生成络合物Fe(SCN)3等。②Fe3+与SCN―以个数比1∶1配合显血红色的络离子为Fe(SCN)2+,该离子与Cl形成络合物[Fe(SCN)]Cl2。③Fe3+与SCN―以个数比1∶5配合,则生成络合离子:[Fe(SCN)5]2-,再根据原子守恒即可写出该反应的化学方程式。④S原子最外层有6个电子,C原子最外层有4个电子,N原子最外层有5个电子,S原子形成1对共价键、C原子形成4对共价键、N原子形成5对共价键从而达到8电子结构,故SCN-电子式为![]() 。
。


科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:同步题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com