
【题目】绿色植物是空气天然的“净化器”,研究发现,1×104 m2柳杉每月可以吸收160 kg SO2,则1×104 m2柳杉每月吸收的SO2分子数目为( )
A. 2 500NA B. 5 000NA C. 7 500NA D. 1 250NA
 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
【题目】在一定温度和压强下,将装有N2和NO2混合气体的试管倒立在水中,经足够的时间后,试管内气体的体积缩小为原体积的3/5,则原混合气体中N2和NO2体积比是
A. 2/3 B. 3/2 C. 3/5 D. 5/3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋动物海鞘中含有种类丰富、结构新颖的次生代谢产物,是海洋抗肿瘤活性物质的重要来源之一。一种从海鞘中提取具有抗肿瘤活性的天然产物的流程如下:
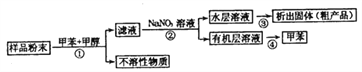
下列关于该流程中各步骤的说法中,错误的是( )
选项 | 步骤 | 采用装置 | 主要仪器 |
A | ① | 过滤装置 | 漏斗 |
B | ② | 分液装置 | 分液漏斗 |
C | ③ | 蒸发装置 | 坩埚 |
D | ④ | 蒸馏装置 | 蒸馏烧瓶 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制500 mL 0.25 mol·L-1的NaOH溶液,试回答下列问题:
(1)计算:需要NaOH固体的质量为_______________。
(2)某学生用托盘天平称量一个小烧杯的质量,称量前把游码放在标尺的零刻度处,天平静止时发现指针在分度盘的偏右位置,此时左边的托盘将________(填“高于”或“低于”)右边的托盘。欲使天平平衡,所进行的操作为_________________________________。
假定最终称得小烧杯的质量为______(填“32.6 g”或“31.61 g”),请用“↓”表示在托盘上放上砝码,“↑”表示从托盘上取下砝码的称量过程,并在标尺上画出游码的位置(画“△”表示)。
砝码质量/g | 50 | 20 | 20 | 10 | 5 |
称量(取用砝 码过程) |
![]()
____________
(3)配制方法:某同学设计了四个操作步骤:
①向盛有NaOH的烧杯中加入200 mL蒸馏水使其溶解,并冷却至室温。
②将NaOH溶液沿玻璃棒注入________中。
③继续往容量瓶中加蒸馏水至液面接近刻度线1~2 cm。
④改用胶头滴管加蒸馏水至刻度线,加盖摇匀。
若按上述步骤配制溶液物质的量浓度会________(填“偏高”“偏低”或“无影响”)。若无影响下面不用填写,若有影响,应在步骤________和步骤________之间,补充的操作是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.硫酸钠溶液和氯化钡溶液反应:Ba2++SO ![]() ═BaSO4↓
═BaSO4↓
B.铜和硝酸银溶液反应:Cu+Ag+═Cu2++Ag
C.铁和稀硫酸反应:2Fe+6H+═2Fe3++3H2↑
D.碳酸钙与稀盐酸反应:CO ![]() +2H+═CO2↑+H2O
+2H+═CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为C、H、0、N、P等元素构成化合物甲、乙、丁及结构丙的示意图,下列说法错误的是
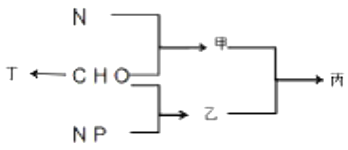
A. 若基因在结构丙上呈线性排列,则甲的单体用双缩脲试剂检测呈紫色
B. 若丁是真核细胞中良好的储能物质,则其合成场所为一种具膜的细胞器
C. 若丙是原核细胞内蛋白质合成场所,则乙彻底水解产物有6种
D. 若丙是一种生物膜,则其功能与膜上甲的种类和数量有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z均为主族元素,分析表中数据,判断下列说法正确的是( )
元素 | X | Y | Z |
最外层电子数 | a | b | a |
原子半径/nm | 0.152 | 0.143 | 0.256 |
A.X与Y位于同一主族,且X在Y的上一周期
B.X与Z位于同一主族,且X在Z的上一周期
C.X与Z位于同一周期,且X的原子序数小于Z的原子序数
D.X与Z位于同一主族,且X的原子序数小于Z的原子序数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了缓解温室效应,科学家提出了多种回收和利用CO2的方案。
方案I:利用FeO吸收CO2获得H2
i.6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) △Hl=-76.0kJ/mol
ⅱ.C(s)+2H2O(g)==CO2(g)+2H2(g) △H2=+113.4kJ/mol (1)3FeO(s)+H2O(g)=Fe3O4(s)+H2(g) △H3=__________。
(2)在反应i中,每放出38.0kJ热量,有______gFeO被氧化。
方案II:利用CO2制备CH4
300℃时,向2L恒容密闭容器中充入2mol CO2和8molH2,发生反应CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g) △H4,混合气体中CH4的浓度与反应时间的关系如图所示。
CH4(g)+2H2O(g) △H4,混合气体中CH4的浓度与反应时间的关系如图所示。

(3) ①从反应开始到恰好达到平衡时,H2的平均反应速率v(H2)=________。
②300℃时,反应的平衡常数K=________。
③保持温度不变,向平衡后的容器中再充入2molCO2和8molH2,重新达到平衡时CH4的浓度_______(填字母)。
A.等于0.8mol/L B.等于1.6mol/L
C.0.8 mol/L <c(CH4)<1.6 mol/L D.大于1.6 mol/L
(4)300℃时,如果该容器中有1.6molCO2、2.0molH2、5.6molCH4、4.0molH2O(g),则v正____v逆(填“>”“<”或“=”)。
(5)已知:200℃时.该反应的平衡常数K=61.8L2·mol-2。则△H4___0(填“>”“<”或“=”)。
方案Ⅲ:用碱溶液吸收CO2
利用100mL3mol/LNaOH溶液吸收4.48LCO2(标准状况),得到吸收液。
(6)该吸收液中离子浓度的大小排序为____________。将该吸收液蒸干,灼烧至恒重,所得固体的成分是_______(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com