
【题目】氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。
Ⅰ.实验室研究氯化钠的性质及制备
(1)氯化钠固体不导电,但氯化钠溶液能导电,用化学用语解释氯化钠溶液能导电的原因:___。
(2)实验室检验Cl-的试剂是___。
(3)某同学用含钠元素的不同类别物质制备NaCl。化学反应方程式如下:
a.2Na+Cl2![]() 2NaCl
2NaCl
b.Na2O+2HCl=2NaCl+H2O
c.
d.Na2CO3+2HCl=2NaCl+CO2↑+H2O
①请补充c反应的化学方程式:___。
②也可用两种盐溶液相互反应获得氯化钠,该反应的化学方程式为___。
Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有Ca2+、Mg2+、SO42-等可溶性杂质。某同学设计了一种制备精盐的实验方案,步骤如下:

(4)写出下列各试剂的化学式
试剂1:___;试剂2:___;试剂3:___。
(5)步骤④中涉及到的离子方程式有:___。
(6)步骤⑦涉及的操作是___。
【答案】NaCl=Na++Cl- AgNO3溶液和稀硝酸 HCl+NaOH=NaCl+H2O Na2SO4+BaCl2=BaSO4↓+2NaCl BaCl2 Na2CO3 HCl Ca2++CO32-=CaCO3↓、Ba2++CO32-=BaCO3↓ 蒸发结晶
【解析】
I.(1)NaCl为强电解质,在溶液中完全电离;
(2)实验室常用硝酸酸化的硝酸银检验Cl-的存在;
(3)①根据反应特点,依次为单质、氧化物、氢氧化物和盐分别与HCl反应制取NaCl;
②可用氯化钙与碳酸钠反应制取氯化钠;
Ⅱ.(4)粗盐除杂时,应先用氯化钡除去硫酸根离子,再除去钙离子、钡离子,可减少操作步骤;
(5)步骤④为除去溶液中的钙离子、钡离子;
(6)氯化钠溶液可用蒸发结晶的方法得到氯化钠。
I.(1)NaCl为强电解质,在溶液中完全电离,生成钠离子和氯离子,则水溶液能导电;
(2)实验室常用硝酸酸化的硝酸银检验Cl-的存在;
(3)①根据反应特点,依次为单质、氧化物、氢氧化物和盐分别与HCl反应制取NaCl,则c为HCl+NaOH=NaCl+H2O;
②可用氯化钙与碳酸钠反应制取氯化钠,方程式为Na2CO3+CaCl2=CaCO3↓+2NaCl;
Ⅱ.(4)粗盐除杂时,应先用氯化钡除去硫酸根离子,再除去钙离子、钡离子,可减少操作步骤,则试剂1为氯化钡溶液,试剂2为碳酸钠溶液,试剂3为盐酸;
(5)步骤④为除去溶液中的钙离子、钡离子,则反应的离子方程式为Ca2++CO32-=CaCO3↓、Ba2++CO32-=BaCO3↓;
(6)步骤⑥得到氯化钠溶液,则步骤⑦可用蒸发结晶的方法得到氯化钠。


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A. (CH3)3C-CH=CH2与氢气完全反应后,生成2,2,3-三甲基戊烷
B. 工业上由乙烯制乙醇、苯制环己烷均属于加成反应
C. C5H11Cl的同分异构体有3种
D.  分子中所有碳原子一定在同一平面上
分子中所有碳原子一定在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中,发生反应NH2COONH4(s)2NH3(g)+CO2(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是
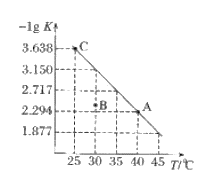
A. 该反应的△H>0
B. C点对应状态的平衡常数K(C)=103.638
C. NH3的体积分数不变时,该反应一定达到平衡状态
D. 30℃时,B点对应状态的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 同一原子中,2p、3p、4p能级的轨道数依次增多
B. 电子排布式(22Ti)1s22s22p63s23p10违反了能量最低原则
C. ![]() 表示的原子能量处于最低状态
表示的原子能量处于最低状态
D. 正三价阳离子的电子排布式为1s22s22p63s23p63d5的元素在周期表中位于Ⅷ族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中不属于氧化还原反应的是
A.NaOH+HCl=NaCl+H2OB.3Fe+2O2![]() Fe3O4
Fe3O4
C.Fe2O3 +3CO![]() 2Fe+3CO2D.2H2O
2Fe+3CO2D.2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含铬(![]() )废水用硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀。该沉淀经干燥后得到nmol FeO·FeyCrxO3。不考虑处理过程中的实际损耗,下列叙述错误的是( )
)废水用硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀。该沉淀经干燥后得到nmol FeO·FeyCrxO3。不考虑处理过程中的实际损耗,下列叙述错误的是( )
A. 消耗硫酸亚铁铵的物质的量为n(2-x)mol
B. 处理废水中![]() 的物质的量为
的物质的量为![]() mol
mol
C. 反应中发生转移的电子数为3nxmol
D. 在FeO· FeyCrxO3中,3x=y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z是第ⅠA~ⅦA族的三种非金属元素,它们在元素周期表中的位置如图所示,试回答下列问题。

(1)X元素单质的化学式是________。
(2)Y元素的原子结构示意图是____________,Y与Na所形成化合物的电子式为________________________。
(3)Z元素的名称是________,从元素原子得失电子的角度看,Z元素具有________性;若从Z元素在元素周期表中所处位置看,它具有这种性质的原因是_________________________,其价电子排布式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】妈妈教小鲁蒸馒头:先用酵头发面,面团发酵至两倍大后,再加纯碱调节酸性,然后将面团揉切后上锅蒸即可。小鲁查阅资料得知,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
(1)下列关于纯碱的认识正确的是___。
A.受热易分解 B.水溶液显碱性 C.属于碱 D.可与酸反应
(2)小鲁探究用Na2CO3调节面团酸度,而不用NaHCO3的原因。
①Na2CO3与NaHCO3质量均为1g时,消耗H+的物质的量更多的是___。
②以Na2CO3或NaHCO3为例,计算消耗H+的物质的量,写出计算过程。___
(3)小鲁实际操作时,发现面团发得不好,面团内的气孔少,略有酸味。妈妈指导小鲁将Na2CO3改用NaHCO3,继续揉面,上锅蒸后果然蒸出了松软的馒头。解释NaHCO3的作用___。
(4)某品牌复合膨松剂的说明书如图所示。

其中葡萄糖酸-δ-内酯和淀粉是助剂,其作用是防止膨松剂吸潮结块而失效。焦磷酸二氢二钠的作用是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分氧化的铁铜合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如下处理:

下列说法正确的是( )
A. 滤液A中的阳离子为Fe3+、Fe2+、H+ B. 样品中Fe元素的质量为2.24g
C. 样品中CuO的质量为4.0g D. V=896
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com