
| A、盐酸 | B、干冰 |
| C、液氯 | D、氯化钠晶体 |
科目:高中化学 来源: 题型:
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用pH试纸测定溶液的pH,应先将pH试纸湿润 |
| B、强酸溶液的导电性一定比弱酸溶液的导电性强 |
| C、SO2溶于水后,水溶液可导电,所以SO2是电解质 |
| D、离子化合物一定是强电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸性:H2SiO3>H2CO3 |
| B、热稳定性:HF>H2O>NH3 |
| C、沸点:HBr>HCl>HF |
| D、离子半径:Na+>F->Li+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④⑥⑧ |
| B、①②⑤⑥⑦ |
| C、②③④⑥⑧ |
| D、③④⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定条件下发生反应E(g)+F(g)═2G(g),该反应△S>0 |
| B、CaCO3(s)═CaO(s)+CO2(g)室温下不能自发进行,说明该反应△H<0 |
| C、一定温度下,反应MgCl2(g)═Mg(l)+Cl2(g)的△H>0,△S>0 |
| D、同一物质:固体→液体→气体的变化时焓增和熵增的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、分子式为C8H10的芳香烃有3个,分别为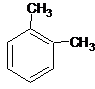 、 、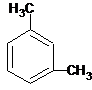 和 和 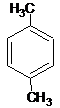 |
| B、分子式为C2H6O的同分异构体有两个,分别是 H3C-O-CH3 和 CH3CH2OH |
| C、分子式为C4H8的烯烃同分异构体有2个,分别为CH2=CHCH2CH3、CH3CH=CHCH3 |
D、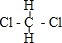 和 和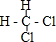 是两种不同的物质 是两种不同的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
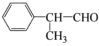 ,工业合成路线如下:
,工业合成路线如下: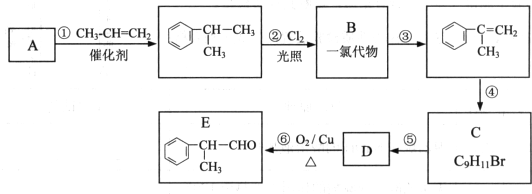
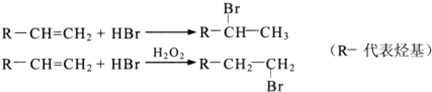
查看答案和解析>>
科目:高中化学 来源: 题型:
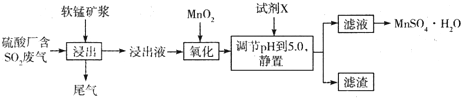
| 离子 | Fe2+ | Fe3+ | Al3+ | Mn2+ |
| 开始沉淀时pH | 7.6 | 2.7 | 3.8 | 8.3 |
| 完全沉淀时pH | 9.7 | 4.0 | 4.7 | 9.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com