
【题目】下列仪器可以加热的是( )
①蒸馏烧瓶;②容量瓶;③蒸发皿;④试管;⑤分液漏斗;⑥量筒;⑦锥形瓶
A.①③④⑦B.②④⑥⑦C.③④⑤D.②③④⑦
科目:高中化学 来源: 题型:
【题目】下列关于金属的说法正确的是( )
A.金属单质在氧化还原反应中常作还原剂
B.金属在加热条件下都易与氧气反应
C.加热条件下铜与硫蒸气反应生成硫化铜
D.铁丝能在氯气中燃烧生成氯化亚铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,水只作氧化剂的是
A. NaH+H2O=NaOH+H2↑ B. Na2O+H2O=2NaOH
C. HCl+NaOH=NaCl+H2O D. 2F2+2H2O=4HF+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的2 L的密闭容器中,加入3 mol A和1 mol B,发生如下反应:3A(g)+B(g)![]() 2C(g)+3D(s),5 min达到平衡时,n(B):n(C) =1:3。
2C(g)+3D(s),5 min达到平衡时,n(B):n(C) =1:3。
(1)0~5 min内用B表示的平均反应速率为_______;达到平衡时,A的转化率为_______。
(2)达到平衡时容器内气体压强与反应前容器内气体压强之比_________。
(3)维持容器的温度不变,若缩小容器的体积,则平衡将向_____(填“正向移动”“逆向移动”或“不移动”)。
(4)达到平衡后,若保持温度不变,将C从容器中分离出一部分,则化学平衡常数____(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的2L密闭容器中,发生反应:X(g)+Y(g)![]() 2Z(g),达到平衡时,各物质的平衡浓度为:c(X)=0.8mol/L;c(Y)=0.1mol/L;c (Z)=1.6mol/L。若用a、b、c分别表示X、Y、Z的起始的物质的量,回答下列问题:
2Z(g),达到平衡时,各物质的平衡浓度为:c(X)=0.8mol/L;c(Y)=0.1mol/L;c (Z)=1.6mol/L。若用a、b、c分别表示X、Y、Z的起始的物质的量,回答下列问题:
(1)若在恒温恒容条件下进行反应X(g)+Y(g)![]() 2Z(g),可判断该反应达到化学平衡状态的是_____
2Z(g),可判断该反应达到化学平衡状态的是_____
A.单位时间内生成n molX的同时生成2nmolZ
B.密闭容器中密度不再改变的状态
C.用X、Y、Z的物质的量浓度变化表示反应速率的比为1∶1∶2的状态
D.反应容器中Y的物质的量分数不再改变的状态
E.密闭容器中压强不再改变的状态
F.混合气体的平均相对分子质量不再改变的状态
(2)a、b应满足的关系是_________。
(3)a的取值范围是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素R、T、X、Y、Z在元素周期表中的相对位置如下图所示,其中Z单质与H2混合遇强光会发生爆炸。则下列判断错误的是
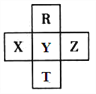
A. 原子半径 Z>Y>R
B. R与Y的电子数相差8
C. 非金属性:Z>Y>X
D. HZO4是目前无机酸中最强的含氧酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是一种重要的有机高分子材料,结构简式为: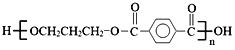 。合成M的一种途径如下:
。合成M的一种途径如下:
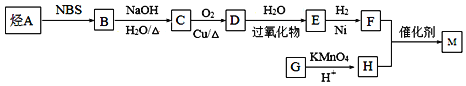
已知:①烃A在标准状况下的密度是1.875g·L-1;②CH3CH2CH=CH2![]() CH3CHBrCH=CH2;③R-CH=CH2+H2O
CH3CHBrCH=CH2;③R-CH=CH2+H2O![]() R-CH2CH2OH;④
R-CH2CH2OH;④![]() 。
。
回答下列问题:
(1)G的结构简式为___________;D中所含官能团的名称为____________________;
(2)A分子中最多有 __________个原子共平面;
(3)D→E反应类型为______________;
(4)写出下列反应的化学方程式:B→C:___________________________;F+H→M:_____________________________________________;
(5)满足以下条件的H的同分异构体有____________种。
①遇FeCl3溶液显紫色 ②可发生银镜反应 ③可与NaHCO3溶液生成CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以Cl2、NaOH、(NH2)2CO(尿素)和SO2为原料可制备N2H4·H2O(水合肼)和无水Na2SO3,其主要实验流程如下:

已知:①Cl2+2OH![]() ClO+Cl+H2O是放热反应。
ClO+Cl+H2O是放热反应。
②N2H4·H2O沸点约118 ℃,具有强还原性,能与NaClO剧烈反应生成N2。
(1)步骤Ⅰ制备NaClO溶液时,若温度超过40 ℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为____________________________________;实验中控制温度除用冰水浴外,还需采取的措施是____________________________________。
(2)步骤Ⅱ合成N2H4·H2O的装置如题19图1所示。NaClO碱性溶液与尿素水溶液在40 ℃以下反应一段时间后,再迅速升温至110 ℃继续反应。实验中通过滴液漏斗滴加的溶液是_____________;使用冷凝管的目的是_________________________________。

(3)步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水Na2SO3(水溶液中H2SO3、![]() 、
、![]() 随pH的分布如题19图2所示,Na2SO3的溶解度曲线如题19图3所示)。
随pH的分布如题19图2所示,Na2SO3的溶解度曲线如题19图3所示)。
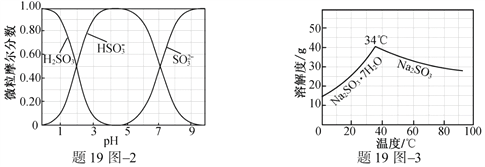
①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定何时停止通SO2的实验操作为_________________。
②请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案: _______________________,用少量无水乙醇洗涤,干燥,密封包装。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com